پنومونی | بیماری های عفونی ریه
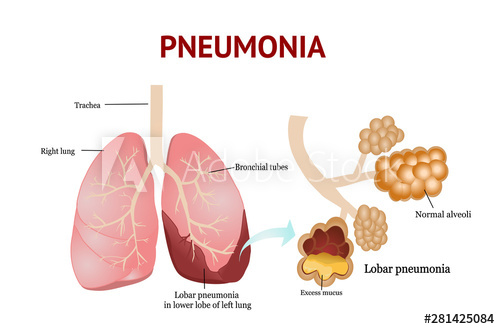
پنومونی
تعریف و اپیدمیولوژی
پنومونی به عنوان عفونت پارانشیم ریه ها تحتانی توسط عواملی مانند باکتریها، ویروسها، قارچ ها، یا حتی انگلها تعریف میشود و باید آن را از پنومونیت که التهاب ریهها ناشی از علل مختلف غیر عفونی شامل مواد شیمیایی، خون، پرتوتابی، و فرایندهای خودایمنی است تمایز داد. پنومونی، علت اصلی مرگ کودکان در سراسر جهان و هشتمین علت مرگ و میر در ایالات متحده است سالیانه مسؤل ۴ تا ۱۰ میلیون عفونت تنفسی است.
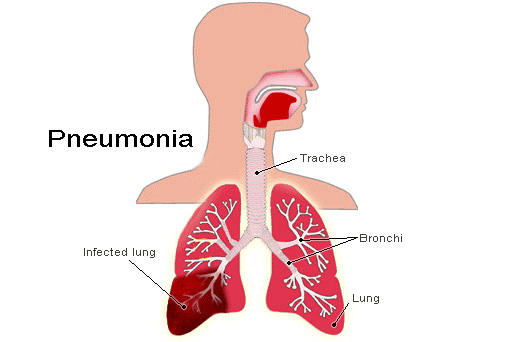
پاتولوژی
عوامل میکروبی میتوانند به طرق مختلف وارد ریهها شوند. مانند فلور طبیعی سینوسها، حلق بینی، حلق دهانی و استنشاق گرد و غبار و گازها از محیط اطراف. شایعترین راه، آسپیراسیون ترشحات دهانی- حلقی است. گونههای لژیونلا، مایکوباکتریومها، قارچهای آندمیک، مایکوپلاسما پنومونیه، کلامیدیا پنومونیه، و اکثر عفونتهای ویروسی مثالهایی از پنومونی ایجاد شده در اثر استنشاق مستقیم ارگانیسمها هستند که منجر به تجمع جغرافیایی و فصلی موارد بیماری میگردد.
با شیوع کمتر، پنومونی از گسترش خونی یا آمبولیک از دریچههای قلبی یا لخته وریدی عفونی ناشی میگردد. عروق کوچک گردش خون ریوی به عنوان صافیهایی برای خون وریدی عمل میکنند که حامل تجمعات کوچک باکتریها از منبعشان میباشد. از این رو پنومونیهای منشاء گرفته از خون اغلب چند کانونی بوده و ضایعات محیطی آن مستعد حفره دار شدن سریع هستند.
علایم بالینی
بیماران معمولاً علایم تنفسی از جمله سرفه خلط دار تنگی نفس، درد سینه، و گهگاه خلط خونی بروز میدهند سایر علایم کمتر اختصاصی عبارتند از: تب، بی حالی فراگیره دردهای عضلانی، و کاهش وزن. تظاهر بیماری ممکن است حاد باشد (در عرض روزها تا هفته ها)، چنانکه در پنومونی باکتریایی دیده میشود، یا تحت حاد و مزمن باشد (در عرض هفتهها تا سال ها)، چنانکه در سل دیده میشود. ممکن است بیماران دچار بی کفایتی سیستم ایمنی (مثل افراد مبتلا به عفونت ویروس نقص ایمنی انسان، مستعد بیماریهای خاص باشند و آگاهی از نقص خاص در سازوکارهای دفاعی میزبان میتواند به تعیین علت عفونت کمک کند.
عکس سینه نقش مهمی ایفا میکند. در بیمار مبتلا به پنومونی یک کدورت پارانشیمی قابل رویت است؛ با این حال بیماریهای غیر عفونی وجود دارند که پنومونی را تقلید میکنند و هیچ یافته پرتونگاشتی، کاملا مختص عفونت نیست.
انتخاب اولیه آنتی بیوتیک ممکن است با هدایت رنگ آمیزی گرم ترشحات تنفسی صورت گیرد. این کار نیازمند نشان دادن یک نمونه خلط رضایت بخش (که به صورت مشاهده بیش از ۲۵ گویچه سفید چند هستهای و کمتر از ۱۰ سلول اپی تلیومی در هر میدان با بزرگنمایی پایین تعریف میشود) و حضور یک ارگانیسم غالب (بیش از ۸ تا ۱۰ ارگانیسم در هر میدان با بزرگ نمایی بالا میباشد، بخصوص اگر همان باکتریها در درون گویچههای سفید نیز یافت شوند. با این حال علی رغم انجام آزمایشات گسترده ارگانیسم مسبب فقط در ۵۰٪ موارد همه پنومونیها قابل شناسایی است. دلیل این امر رنگ پذیری ضعیف باکتریهایی مثل لژیونلا پنوموفیلا، کلامیدیا پنومونیه، عدم وجود دیواره پپتیدوگلیکان در مایکوپلاسما پنومونیه و ارگانیسمهای مختلفی که به سختی کشت میشوند و نتایج کشت در آنها قطعی نیست. جدول ۱-۲۱ شایعترین عوامل مسؤل عفونتهای ریوی را نشان میدهد.
دستورالعملهای بالینی برای در اختیار نهادن یک رویکرد نظام مند به تشخیص و درمان پنومونی ایجاد شدهاند. یک سوال کلیدی که باید در ارزیابی اولیه پنومونی پرسیده شود این است که آیا پنومونی اکتسابی از جامعه میباشد یا مرتبط با مراقبتهای بهداشتی؟
تشخیص افتراقی، درمان و پیشآگهی
پنومونی اکتسابی از جامع
پنومونی اکتسابی از جامعه در زمستان دو برابر شایعتر است و افرادی که در دو انتهای طیف سنی (زیر ۵ سال و بالای ۶۵ سال) قرار دارند در معرض خطر بیشتری هستند. شایعترین عامل مسبب استرپتوکک پنومونیه، یک باکتری دیپلوککا گرم مثبت است که ساختار کپسول دارش و IgA پروتئاز آن را از دفاع میزبان محافظت ممکن است بیماران یک عفونت پیشین تنفسی فوقانی داشتهاند که به دنبال آن حمله ناگهانی تب، لرز تکان دهنده، تنگی نفس، و پلورزى عارض گشته است. سرفه همراه با خلط قهوهای مایل به قرمز شایع است. مطالعات تصویربرداری تراکم لوبار را نشان میدهند. رنگ آمیزی گرم خلط فقط در ۴۵٪ مواردی که باکتریمی دارند مثبت است. به همین سبب تشخیص با کشت ارگانیسم از یک محل معمولاً عاری از میکروب مثل خون، مایع جنبی، یا مایع مغزی-نخاعی مسجل میگردد. در بسیاری از موارد تشخیص با گمانه زنی است و پوشش انتی بیوتیکی توصیه شده برای پنومونی اکتسابی از جامعه به منظور پوشش این ارگانیسم است (به مطالب بعدی مراجعه کنید).
مایکوپلاسما پنومونیه یک ارگانیسم بی هوازی اختیاری کند رشد است که عامل ۲۵ تا ۶۰ درصد همه پنومونیهای غیرمعمول میباشد. مایکوپلاسما پنومونیه علت شایع پنومونی در بیماران ۵ تا ۳۵ ساله است که ممکن است در ابتدا علایم تنفسی فوقانی، فارنژیت، و التهاب تاولی پرده صماخ را بروز دهند. سرفه خشک، تب، علایم گوارشی، سردرد، و دردهای عضلانی شایع هستند. عوارض ناشایع عبارتند از: همولیز ناشی از آگلوتینین سرد، هپاتیت، اریتم مولتی فرم، سندرم ترشح نابه جای هورمون ضدادراری، پریکاردیت، میوکاردیت، و ناهنجاریهای نورولوژیک. ممکن است عکس سینه ارتشاح تورینهای-گرهکیه بینابینی ظریف در بیماران که اغلب نسبتاً بدون علامت هستند نشان دهد. تشخیص براساس ویژگیهای بالینی و همه گیر شناختی داده میشود. برای اثبات تشخیص، یافتههای سرم شناختی مرحله حاد و دوره نقاهت ضرورت دارند اما در بیماری حاد کمک کننده نمیباشند.
سایر علل شایع پنومونی اکتسابی از جامعه را کلامیدیا پنومونیه و هموفیلوس آنفلونزا تشکیل میدهند. بیماران دچار هم ابتلایی و آنهایی که بیش از ۶۵ سال سن دارند در معرض خطر پنومونی ناشی از گونههای لژیونلا، استافیلوکک طلایی، و ارگانیسمهای گرم منفی نیز میباشند. هنگامی که مقادیر زیادی از ترشحات دهانی- حلقی در بیماران دچار عفونت مزمن لثه أسپیره میشوند باید عفونت بی هوازی مدنظر باشد.
علل ویروسی ممکن است تا ۶۵٪ از موارد پنومونی اکتسابی از جامعه را در شیرخواران و کودکان پیش از دبستان کمتر از ۵ سال) سبب شوند. شایعترین پاتوژنهای شناسایی شده، رینوویروس، ویروس پارا آنفلونزا، آدنوویروس، انتروویروس، کرونا ویروس، متا پنوموویروس انسانی (hMpv) و ویروس سن سیشیال تنفسی (RSV) هستند. HMPV اخیرا به فهرست بلند علل ویروسی اضافه شده و اغلب در بچههای کوچک و سالمندان درگیری مجاری هوایی فوقانی و تحتانی میدهد. این ویروس در اواخر زمستان واوایل بهار شایع است. یعنی زمانی که RSV شایع است و عفونت همزمان HMPV با RSV سبب برونشیولیت شدید در بچههای زیر ۲ سال میشود.
در سپتامبر ۲۰۱۲، یک بتاکروناویروس جدید از مردی در عربستان سعودی جدا شد. سندرم تنفسی خاورمیانه یا MERS – COV سبب پنومونی حاد شدید، سندرم زجر تنفسی حاد (ARDS) و آسیب حاد کلیه میشود. این ویروس تاکنون در اروپا و سایر بخشهای خاورمیانه هم شناسایی شده است. بیماران ممکن است علایم گوارشی، پریکاردیت و انعقاد داخل عروقی منتشر (DIC) نیز پیدا کنند. تشخیص کرونا ویروس مرس با انجام PCR و عفونت زایی آن بر اساس آنتاگونیز کردن تولید اینترفرون آندوژن در سلولها تأیید میشود. درمان حمایتی است و با کمک تهویه مکانیکی و اکسیژناسیون غشایی خارج تنهای (EMCO) انجام میشود، اما اینتر مزون آلفا ۲b تکثیر ویروس را در محیط آزمایشگاه کاهش داده است. میزان مرگ و میر کرونا ویروس مرس تا ۴۸٪ است که به طور متوسط ۱۴ روز پس از ظهور علایم بالینی اتفاق میافتد.
آزمایشات تشخیصی برای پنومونی اکتسابی از جامعه باید شامل عکس سینه و شمارش کامل خون باشند. نقش کشتهای رایج خون و خلط در این زمینه محل اختلاف نظر است. م طالعات از پروتئین واکنشی (CRP)C و پروکلسیتونین به عنوان نشانههای پاسخ التهابی به عفونت باکتریایی حمایت کردهاند. اما بررسیهای بیشتری – مورد نیاز است.
درمان توصیه شده برای پنومونی اکتسابی از جامعه یک دوره (۷ تا ۱۰ روزه) از یک آنتی بیوتیک ماکرولید (اریترومایسین، کلاریترومایسین، یا آزیترومایسین) میباشد. آزیترومایسین به ویژه در بیمارانی که خطر بیماری قلبی- عروقی در آنها بالا است، با افزایش احتمال مرگ قلبی- عروقی همراه بوده است. اگر هم ابتلاییهایی مثل بیماری مزمن قلب یا ریه وجود داشته باشد باید از یک فلوروکینولون وسیع الطیف (مثل لووفلوکساسین، موکسی فلوکساسین، یا جمی فلوکساسین) یا یک بتالاکتام (آموکسی سیلین) به علاوه یک ماکرولید استفاده کرد. انتخاب درمان باید از الگوهای مقاومت آنتی بیوتیکی ناحیه هم تأثیر پذیر باشد.
تصمیم مهم در مراقبت از پنومونی اکتسابی از جامعه این است که آیا بیمار نیازمند پذیرش در بیمارستان هست یا خیر؟ این تصمیم باید با مد نظر قرار دادن عوامل خطر شناخته شده برای افزایش مرگ و میر ناشی از پنومونی اتخاذ گردد. این عوامل عبارتند از: سن ۶۵ سال یا بالاتر؛ وجود هم ابتلاییهایی مثل دیابت قندی، نارسایی کلیه، یا نارسایی احتقانی قلب؛ تغییر وضعیت روانی؛ تاکیکاردی (بیشتر از ۱۲۵ ضربان در دقیقه)؛ افزایش تعداد تنفسه (بیشتر از ۳۰ تنفس در دقیقه)؛ تب بالا (بیشتر از ۳/۳۸ تا ۴۰ درجه سلسیوس)؛ افت فشار خون (فشار خون سیستولی کمتر از ۹۰ میلی متر جیوه)؛ هیپوکسی (۹۰٪ > Sao۲ یا mmHg60 < Pao۲)؛ درگیری چند لوب در عکس سینه؛ و شناسایی عوامل بیماری زای پرخطر مثل ارگانیسمهای گرم منفی و استافیلوکک طلایی.
برای بیماران بستری درمان اولیه پنومونی اکتسابی از جامعه معمولاً شامل یک سفالوسپورین مثل سفتریاکسون یا سفوروکسیم بایا بدون یک ماکرولید است. درمان آنتی بیوتیکی باید هر چه زودتر آغاز گردد چون مرگ ومیر میتواند حتی پس از تأخیر کوتاه (بیشتر از ۸ ساعت) در دریافت آنتی بیوتیک مناسب افزایش یابد. باید قبل از شروع درمان آنتی بیوتیکی کشت خلط و خون اخذ گردد.
پنومونی بیمارستانی
پنومونی بیمارستانی به سه زیرگروه تقسیم بندی میشود: پنومونی اکتسابی از بیمارستان (HAP پنومونی مرتبط با دستگاه تهویه مصنوعی (VAP) و پنومونی مرتبط با مراقبت بهداشتی (HCAP). پنومونی اکتسابی از بیمارستان بصورت یک پنومونی که ۴۸ ساعت یا بیشتر پس از پذیرش [در بیمارستان] عارض میگردد، تعریف میشود. پنومونی مرتبط با دستگاه تهویه مصنوعی نوعی پنومونی اکتسابی از بیمارستان است که بیشتر از ۴۸ تا ۷۲ ساعت پس از لولهگذاری داخل نای عارض میگردد. پنومونی مرتبط با مراقبت بهداشتی بصورت یک پنومونی تعریف میشود که در فردی اتفاق میافتد که بستری نبوده اما تماس زیادی با مراقبین بهداشتی داشته است و شامل بستری اخیر در بیمارستان، سکونت در آسایشگاه سالمندان با سایر مکانهای نگهداری طولانی مدت، و درمان داخل وریدی اخیر میباشند. این بیماران باید در معرض خطر بالا برای ابتلا به ارگانیسمهای مقاوم و در نتیجه نامناسب برای درمان رایج تجربی برای پنومونی اکتسابی از جامعه در نظر گرفته شوند.
پنومونی بیمارستانی دومین عفونت شایع در بیماران بستری و شایعترین عفونت در واحد مراقبتهای ویژه (ICU) میباشد. بیماریزایی پنومونی بیمارستانی بر پایه استقرار عوامل بیماری زا در حلق دهانی و معده و متعاقبا آسپیراسیون این ارگانیسمها به درون دستگاه تنفس تحتانی میباشد. با خنثی سازی اسید معده استقرار ارگانیسمهای گرم منفی در معده افزایش مییابد. در پنج روز اول پس از بستری اغلب هموفیلوس آنفلونزا، استرپتوکک پنومونیه، و استافیلوکک طلایی جدا میشوند. پس از این مدت پنومونی اغلب توسط سودومونا آیروژینوزا، استافیلوکک طلایی، میکروبهای بی هوازی، گونههای آسینتوباکتر، و انواع باسیلهای گرم منفی رودهای ایجاد میشود. این یافته نتایج درمانی مهمی در بر دارد چرا که این ارگانیسمها به طور شایعتری با مقاومت به چند داروی آنتی بیوتیک همراه میباشند. درمان با ترکیبی از پنی سیلین بتالاکتام ضد سودمونا یا سفالوسپورین و یک آمینوگلیکوزید یاکینولون صورت میگیرد. در صورت شک به استافیلوکک طلایی مقاوم به متی سیلین، ونکومایسین اضافه میگردد. اغلب در این بیماران با استفاده از روشهای تهاجمیتر مثل مکش از لوله داخل نای در بیمارانی که لولهگذاری شدهاند یا برونکوسکوپی فیبر نوری قابل انعطاف به دنبال شناسایی دقیقتر ارگانیسمها و حساسیت آنها به آنتی بیوتیکها میگردیم. با این حال به نظر میرسد بهترین پیش بینی کننده سرانجام بیمار مبتلا پنومونی اکتسابی از بیمارستان کفایت رژیم آنتی بیوتیکی تجربی اولیه میباشد.
عوارض پنومونی
تراوش جنبی ناشی از پنومونی یک تراوش جنبی اگزودایی نوتروفیلی در مجاورت ریه مبتلا به پنومونی میباشد. این تراوش مراحل اگزودایی، فیبرینی چرکی و ارگانیزه شده دارد. بسته به مرحله آن میتوان این وضعیت را با آنتی بیوتیک به تنهایی درمان کرد؛ یا ممکن است علاوه بر آنتی بیوتیکها محتاج تخلیه نیز باشد. با پیشرفت پنومونی مایع التهابی ریه به درون فضای جنبی نشت میکند که در ابتدا به صورت یک تراوش جنبی بدون عارضه تظاهر مییابد (یعنی مرحله اگزودایی). در این نقطه تراوش جنبی با درمان آنتی بیوتیکی تنها بهبود خواهد یافت. در طی مراحل فیبرینی چرکی و ارگانیزه شده، فرایند التهابی با متابولیسم بی هوازی، تولید سیتوکین، انباشت فیبرین در فضای جنب، و ضخیم شدن پرده جنب مشخص میشود.
یک تعریف پذیرفته شده توسط همگان در مورد آمپیم وجود ندارد. با این حال اکثر پزشکان همه تراوشهای جنبی را که واضحأ چرکی بوده یا حاوی میکروارگانیسمهایی هستند که توسط رنگ آمیزی گرم یا کشت تشخیص داده میشوند در اصطلاح آمپیم میگنجانند. آمپیم همیشه باید با تخلیه حفره جنب معمولاً توسط یک لوله توراکوستومی قرار داده شده در قفسه سینه درمان شود. تراوشهای جنبی ناشی از پنومونی که به شدت التهابی هستند ممکن است به گونهای رفتار کنند که انگار عفونی هستند گرچه میکروارگانیسمها هرگز شناسایی نمیشوند. تراوشهای جنبی که به عنوان تراوش جنبی عارضه دار ناشی از پنومونی توصیف میشوند از نظر بالینی با pH زیر ۷٫۱، لاکتات دهیدروژناز بالای سرم (LDH) و میزان گلوکز کمتر از ۴۰ میلی گرم در دسیلیتر تشخیص داده میشوند. تراوشهای جنبی عارضه دار عموماً علاوه بر درمان آنتی بیوتیکی نیازمند تخلیه نیز هستند.
عامل خطر اصلی ایجاد آبسه ریوی، آسپیراسیون است که منجر به عفونت چند میکروبی موذیانهتری میگردد که معمولاً هم شامل هوازیها و هم بی هوازیها میباشد. شرایطی که بیمار را مستعد آسپیراسیون میسازند (مثل الکلیسم، تشنج، یا سکته مغزی با افزایش میزان بروز آبسه ریوی همراه هستند. داشتن دندانهای فاسد بار باکتریهای بی هوازی در دهان و نتیجتا احتمال عفونت پس از آسپیراسیون را افزایش میدهد. در کار آزماییهای درمان تجربی آبسه ریه احتمالاً به خاطر بروز ۱۵ تا ۲۰ درصدی بی هوازیهای مقاوم به پنی سیلین در آبسههای ریوی، کلیندامایسین نسبت به پنی سیلین برتری نشان داد. آنتی بیوتیکها باید برای ۶ ماه ادامه داده شوند و تخلیه باید برای آبسههای بسیار بزرگ یا عدم بهبود با آنتی بیوتیکها نگه داشته شود.
عفونت با مایکوباکتریوم توبرکلوزیس
عفونت با مایکوباکتریوم توبرکلوزیس، یک باسیل هوازی، بی حرکت، و مقاوم در برابر رنگزدایی با اسید و تولیدکننده نیاسین باعث سل میشود. در سال ۲۰۱۱ پروژه مراقبت و پایش جهانی سازمان بهداشت جهانی ۸٫۷ میلیون مورد جدید ابتلا به سل در سال تخمین زد که ۱۳٪ از آنها همزمان عفونت HIV نیز داشتند. ۱۲ میلیون بیمار از قبل و عمدتاً در آسیا و آفریقا وجود داشت. سالیانه ۱٫۴ میلیون نفر در اثر بیماری سل جان میسپارند و میزان مرگ و میر موردی در جهان ۲۳٪ است که در برخی کشورهای آفریقایی با میزان بالای عفونت با ویروس نقص ایمنی اکتسابی انسان (HIV) به ۵۰٪ میرسد. در ایالات متحده سل به علت افزایش ناگهانی عفونت HIV، سوءمصرف مواد، فقر در مرکز شهر، و بی خانمانی به میزان هشداردهندهای در اوایل دهه ۱۹۹۰ افزایش پیدا کرد.
عفونت سل زمانی رخ میدهد که قطرههای آلودهای که به صورت ذرات معلق در آمدهاند (در اثر دفع خلط توسط فرد بیمار توسط فرد دیگری تنفس میشوند و هسته قطرک به حبابچه میرسد. این عفونت تقریباً همیشه نهفته است که عفونت سلی نهفته نامیده میشود. اگر سیستم ایمنی ذاتی۴ میزبان از حذف عفونت نهفته عاجز باشد باسیلها در درون ماکروفاژهای حبابچهای تکثیر مییابند و سلوها را میکشند. ماکروفاژهای عفونی شده سیتوکین و کموکین تولید میکنند که سایر سلولهای فاگوسیتی شامل منوسیتها، سایر ماکروفاژهای حبابچهای، و نوتروفیلها را جذب میکنند و نهایتاً یک ساختمان گرانولومی گرهکی به نام توبرکول ایجاد میکنند. اگر تکثیر باکتری کنترل نشود توبرکول بزرگ شده و باسیلها به گرههای لنفاوی تخلیه کننده موضعی وارد میشوند که منجر به لنفآدنوپاتی، یک تظاهر شاخص سل اولیه میگردد.
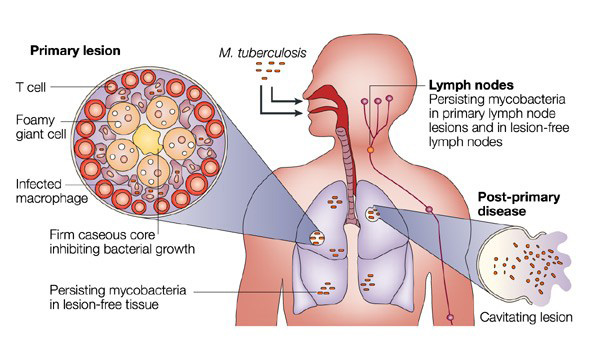
ضایعه ایجاد شده در اثر توسعه توبرکول به داخل پارانشیم ریه و درگیری گره لنفاوی، کمپلس گانه خوانده میشود. باکتریها تا زمانی که یک پاسخ ایمنی کارآمد با واسطه سلول که معمولاً ۲ تا ۶ هفته پس از عفونت ایجاد میگردد رخ ندهد به تکثیر خود ادامه میدهند. ناتوانی میزبان در ترتیب دادن یک پاسخ ایمنی کار آمد با واسطه سلول و ترمیم بافتی، منجر به تخریب پیشرونده ریه میگردد. محصولات باکتریایی، عامل نکروزکننده تومور آلفا (TNFa)، مولکولهای دارای اثر ضد میکروبی ماکروفاژ مثل واسطههای واکنشگر اکسیژن و واسطههای واکنشگر نیتروژن و محتویات سلولهای سیتوتوکسیک (گرانزیمهای پرفورین) همگی میتوانند در ایجاد نکروز پنیری که مشخصه گرانولوم سلی است دخیل باشند. و اگر رشد مایکوباکتریومها مهار نشده و ادامه یابد ممکن است باسیلها از طریق خون گسترش یافته و سل منتشر ایجاد کنند. سل ارزنی یک شکل منتشر سل میباشد که ضایعات آن شبیه دانه ارزن هستند. باسیلها میتوانند از طریق مکانیکی با خوردگی ضایعات به درون مجاری هوایی ریه نیز گسترش یابند. در این نقطه است که میزبان برای دیگران عفونت زا میباشد.
در صورت عدم درمان ۸۰٪ بیماران فوت خواهند کرد. سایرین دچار بیماری مزمن شده یا خودبه خود بهبود مییابند. مشخصه بیماری مزمن، دفعات مکرر التیام خودبه خود همراه با تغییرات فیبروتیک در اطراف ضایعه و تخریب بافت میباشد. التیام با ریشه کنی خود به خودی کامل باسیلها نادر است.
فعال شدن دوباره سل زمانی رخ میدهد که باکتریهای پایدار در بدن میزبان یکباره شروع به تکثیر میکنند. فقط ۵ تا ۱۰ درصد بیمارانی که دچار هیچ مشکل طبی زمینهای نیستند و دچار عفونت میشوند در طول زندگی خود به بیماری ناشی از فعال شدن دوباره مبتلا میگردند. گرچه به وضوح سرکوب ایمنی با فعال شدن دوباره سل ارتباط دارد اما روشن نیست که چه عواملی در میزبان به طور خاص عفونت را سالها در وضعیت نهفته نگه داشته و چه چیزی باعث آشکار شدن عفونت نهفته میگردد.
تشخیص عفونت سل نهفته بستگی به آزمایش توبرکولین مثبت دارد که الزاما نشان دهنده بیماری فعال نیست و فقط عفونت قبلی را نشان میدهد. آزمایش استاندارد مانتو عبارت است از تزریق داخل جلدی ۱/۰ میلی لیتر (۵ واحد توبرکولین) PPD در پوست ساعد. محل تزریق ۴۸ تا ۷۲ ساعت بعد ارزیابی میشود. خواندن نتیجه بر مبنای قطر ناحیه سفت شده یا برآمده میباشد.
بیماران مدت کوتاهی پس از تبدیل توبرکولین در معرض خطر بالای ابتلا به سل فعال قرار دارند و به همین سبب درمان عفونت سلی نهفته توصیه میشود. کوانتی فرون طلایی
(QFt-G) جهت تشخیص عفونت نهفته سلی (LTBI) و سل توسط سازمان غذا و داروی ایالات متحده تأیید شده است. کوانتی فرون از دو پروتئین موجود در و مایکوباکتریوم توبرکلوزیس (یعنی ESAT6 و CFP10) استفاده کرده و به روش ELISA انجام میشود. به دلیل اینکه این پروتئینها در همه گونههای واکسن BCG وجود ندارند، این آزمون سبب نتایج مثبت کاذب در افرادی که قبلاً با واکسن BCG دریافت کرده اند، نمیشود. مزایای دیگر کوانتی فرون این است که نتایج آن در عرض ۲۴ ساعت و بدون نیاز به ویزیت دوم و اشتباهات خواندن تست در دسترس میباشد. این آزمون همچنین مانند آزمون پوستی توبرکولین (TST) در افتراق بیماری سل و عفونت نهفته سلی محدود عمل میکند. افتراق این دو مورد بر اساس علایم مشکوک، تصویربرداری و نمونههای خلط داده میشود. کوانتی فرون منفی نمیتواند عدم وجود عفونت سل در بیمارانی که علایم و نشانههای سل را دارد، آنها که HIV مثبت هستند یا آنهایی که ضعف ایمنی شدید دارند را رد نماید.
خطر بیماری فعال در عرض ۲ سال پس از مواجهه ۵٪ و پس از آن ۵٪ در سال میباشد. بیماران مبتلا به HIV استثناء هستند و در عرض چند ماه پس از تبدیل با ۴۰٪ خطر بیماری فعال مواجه میباشند. توصیههای فعلی در مورد اینکه چه چیز یک آزمایش PPD مثبت تلقی میشود درجه شک بالینی به عفونت سلی نهفته را مد نظر قرار میدهد (جدول ۲-۲۱). درمان معمول عفونت سلی نهفته، mg/kg 5 تا حداکثر mg ۳۰۰ در روز ایزونیازید به مدت ۹ ماه میباشد (بزرگسالان).
درمان افراد مشکوک به بیماری فعال حداقل شامل چهار دارو میباشد (ایزونیازید، mg/kg 5 در روز؛ ریفامپین mg/kg 10 در روز؛ اتامبوتول mg/kg 20-15 در روز؛ پیرازینامید، mg/kg 30-15 در روز) و باید قبل از رسیدن به یک تشخیص رسمی مد نظر قرار گیرد. عواملی که مطرح کننده بیماری فعال هستند شامل مواجهه با سل فعال، علایم ریوی، و بیماری حفره دار در بررسی تصویربرداری میباشند. در صورت مسجل شدن تشخیص سل داروها به مدت ۲ ماه ادامه داده میشوند مگر عوارض ناشی از درمان دارویی عارض گردد. پس از ۲ ماه، بسته به مطالعات حساسیت دارویی [مایکوباکتریومها] میتوان رژیم دارویی را متناسب با آن تغییر داد و حداقل با دو داروی فعال برای ۴ ماه دیگر ادامه داد. میزان [شیوع] سل مقاوم به دارو در جمعیتهای خاص (مثل مهاجرین اخیر از نواحی با میزان بالای ابتلا به سل، افراد بی خانمان) افزایش دارد.
مقاومت [به دارو] در ۹٪ بیمارانی که قبلاً درمانی دریافت نکردهاند و در ۸/۲۲% آنها که درمان قبلی دریافت نمودهاند یافت میشود. در بیمارانی که مبتلا به سل مقاوم به دارو هستند درمان باید حداقل شامل سه دارویی باشد که قبلاً تجویز نشده و ارگانیسم در آزمایشگاه به آنها حساس است. درمان حداقل باید برای ۱۸ تا ۲۴ ماه ادامه پیدا کند. نظارت مستقیم بر درمان (DOT) برای اطمینان از پذیرش از جانب بیماران توصیه میشود.
پنومونی پنوموسیستیس
پنوموسیستیس جیرووکی (pcp) که قبلاً پنوموسیستیس کارینی نامیده میشد یک قارچ فرصت طلب است که در دوران قبل از سندرم نقص ایمنی اکتسابی (AIDS) عمدتاً در نوزادان نارس دچار سوء تغذیه و بزرگسالان مبتلا به بدخیمی خونی که تحت شیمی درمانی قرار میگرفتند رخ میداد. به هر حال میزان بروز آن در اواخر دهه ۱۹۸۰ و دهه ۱۹۹۰ در بیماران مبتلا به AIDS که شمارش لنفوسیت +CD4 پایین (mm۳/سلول ۲۵۰ >) داشتند به میزان قابل توجهی افزایش یافت.
ممکن است بیماران از سرفه بدون خلط، تب، تنگی نفس، و کاهش وزن شکایت داشته باشند. علایم در بیماران مبتلا به HIV پیشرفت تدریجی طی هفتهها دارد. کاندیدیاز دهان، افزایش لاکتات دهیدروژناز (LDHI) سرم، افزایش شیب اکسیژن حبابچهای – شریانی، و کاهش شمارش النفوسیت های) *CD4 پیشگوی کنندههای مستقل پنومونی پنوموسیستیس مرتبط با HIV هستند.

تصاویر پرتوشناختی از قفسه سینه ممکن است نشان دهنده ارتشاح بینابینی دوطرفه منتشر باشند اما ممکن است در قریب به ۱۵٪ بیماران چیزی دیده نشود. توموگرافی کامپیوتری با وضوح بالا (HRCT)، حساستر بوده و دقت تشخیصی آن برای PCP، ٪۹۴ است. سایر یافتهها عبارتند از ارتشاحهای منفرد، ضایعات حفره دار ، تودههای گرهکی، پنوموتوراکس و تابلوی ارزنی. لنفآدنوپاتی ناف ریه و مدیاستن نادر میباشد. شناسایی ارگانیسم در خلط که در ۶۰ تا ۸۵ درصد از بیماران کارایی دارد در تشخیص کمک کننده خواهد بود. برونکوسکوپی همراه با شستشوی برونشی- حبابچهای میتواند بازده را افزایش دهد (۸۶٪)، بخصوص اگر یک نمونه از طریق برونش نیز برداشته شود (۹۸ تا ۱۰۰ درصد).
می توان توسطتری متوپریم سولفامتوکسازول خوراکی یا پنتامیدین استنشاقی پیشگیری کرد. وقتی پنومونی وجود دارد درمان انتخابیتری متوپریم سولفامتوکسازول است. با این حال عوارض ناخواسته قابل توجهی اعم از کاهش گویچههای سفید خون (لکوپنی)، تهوع، استفراغ، و افزایش ترانس آمینازهای کبدی با این درمان همراه هستند. پنتامیدین وریدی جایگزین قابل قبولی برایتری متوپریم سولفامتوکسازول میباشد اما این درمان میتواند با عارضه افت قند خون (هیپوگلسیمی) همراه باشد. رژیمهای دارویی با سمیت کمتر در دسترس میباشند (مثل
تری متوپریم و داپسون، کلیندامایسین و پریماکین) اما این رژیمهای درمانی فقط پس از شکست سایر داروها قابل توصیه میباشند. در مبتلایان به بیماری شدید که با هیپوکسمی قابل توجه (مثلاً mmHg 70 Pao۲<) مشخص میگردد باید کورتیکواستروئیدها را مد نظر قرار داد. کورتیکواستروئیدها احتمال پیشرفت به سمت نارسایی تنفسی را کاهش میدهند.
چشم اندازهای آینده
عفونتهای ریوی همچنان منبعی برای میزان بالای مرگ و میر و عوارض، هم در جامعه و هم در محیط مراقبتهای بهداشتی میباشند. بخش قابل توجهی از این عفونتها در انتهای طیف سنی (کودکان و بزرگسالان سالمند) را درگیر میکنند. استفاده عاقلانه از داروهایی که در حال حاضر در دسترس میباشند از ایجاد مقاومت دارویی پیشگیری کرده یا آن را به تأخیر میاندازد. تلاشهای مستمر برای تحکیم تزریق واکسن علیه عوامل عفونی از جمله آنفلونزا و استرپتوکک پنومونیه لازم است.
عفونت همزمان HIV و سل همچنان مشکل عمدهای در آفریقا میباشد، جایی که درمان مؤثر علیه HIV کمتر قابل دسترس است. اهمیت این نکته با شناسایی سل شدید مقاوم به دارو ( XDR – Tb) که توسط گونهای از مایکوباکتریوم توبرکلوزیس مقاوم به بسیاری از داروهای ضد مایکوباکتریایی در دسترس ایجاد میگردد و درمان آن مشکل میباشد مورد تأکید قرار گرفته است. نگرانیهایی در مورد عوارض جانبی ایمنسازی هم وجود دارد.
همه گیریهای جدید و مرگباری همچنان شناسایی میشوند، مثلاً کروناویروس مرس (MERS-CoA) MERS و یک سندرم تنفسی حاد شدید (SARS). سارس یک بیماری تنفسی سریعا پیشرونده است که در استان گوانگدونگ چین، هنگ کنگ، ویتنام، سنگاپور و کانادا شناسایی شد.
طی قرن گذشته ۴ عالمگیری توسط انفلونزا رخ داده است که هر یک به علت ظهور یک ویروس آنفلونزای جدید بوده است و اخیرا ویروسهای جدید حاوی اجرایی از ویروس آنفلونزای انسان و پرندگان بودند. تخمینها از مرگ و میر بالقوه جهانی در ارتباط با آنفلونزای عالمگیر پرندگان در حد ۶۲ میلیون مورد مرگ میباشد و در حال حاضر هیچ درمان خاصی در دسترس نمیباشد. در سال ۲۰۰۹ ویروس انفلونزای یک HIN1 ( خوکی) در مکزیک ظهور کرد، در H1N1 سرتاسر جهان پخش شد و رسما از طرف با WHO عالمگیری لقب گرفت. حداقل در ابتدا مرگ و میر (ویروس نسبتاً پائینی همراه بوده است اما محتمل است که این ویروس آنفلونزا جهش پیدا کرده و بیماری شدیدتری در انسانها ایجاد کند. جدیدترین طغیان آنفلونزای A پرندگان، گونه H7N9 بود که در سال ۲۰۱۳ محدود به چین بود و اغلب بیماران تماس با ماکیان (مرغ و خروس) را گزارش کردند و مدرکی از انتقال پایدار انسان به انسان وجود نداشت. تعیین توالی ژنهای ۱۶S rRNA با انجام واکنش زنجیرهای پلی مراز (PCR) ممکن است برای شناسایی باکتریها مفید باشد. فرضیه dysbiosis میگوید تغییر در ساختار و پایداری جمعیتهای میکروبی ممکن است سبب بیماری در انسان شود. در مورد ریه، جایی که قبلاً گمان میشد استریل باشد، تعیین توالی ژن ۱۶S rRNA یک نگاه اجمالی به میکروبیوم طبیعی دستگاه تنفس را فراهم کرده است. بر پایه تغییر در این جمعیتهای میکروبی، پی به علت، تشخیص و درمان انواع بیماریها خواهیم برد.
منابع
American Thoracic Society, Infectious Diseases Society of America: Guidelines for the management of adults with hospital acquired, ventilator-associated, and healthcare-associated pneumonia, Am J Respir Crit Care Med 171:388 416, 2015.
Blumberg HM, Burman WJ, Chaisson RE, et al: American Thoracic Society/ Centers for Disease Control and Prevention/Infectious Diseases Society of America: treatment of tuberculosis. Am J Respir Crit Care Med 167:603-662, 2003.
Kovacs JA, Gill J, Meshnick S, et al: New insights into transmission, diagnosis, and drug treatment of Pneumocystis carinii pneumonia, JAMA 286:2450-2460, 2001.
Mandell LA, Wunderink RG, Anzueto A, et al: Infectious Diseases Society of America/American Thoracic Society consensus guidelines on the management of community-acquired pneumonia in adults, Clin Infect Dis 44S:S27-S72, 2007.
Mazurek GH, Villarino ME, CDC: Guidelines for using the QuantiFERON-TB test for diagnosing latent Mycobacterium tuberculosis infection. Centers for Disease Control and Prevention, MMWR Recomm Rep 52:15-18, 2003.
Disease Control and Prevention, MMWR Recomm Rep 52:15-18, 2003.
Partinen M, Saarenpää-Heikkilä O, Ilveskoski I, et al: Increased incidence and clinical picture of childhood narcolepsy following the 2009 HINI pandemic vaccination campaign in Finland, PLOS ONE 7:e33723, 2012.
Stolz D, Stulz A, Muller B, et al: BAL neutrophils, serum procalcitonin, and C reactive protein to predict bacterial infection in the immunocompromised host, Chest 132:504-514, 2007.
Tsolia MN, Psarras S, Bossios A, et al: Etiology of community-acquired pneumonia in hospitalized school-age children: evidence for high prevalence of viral infections, Clin Infect Dis 39:681-686, 2004.

مبانی طب داخلی سیسیل
مشاوره : اگر نیاز به مشاوره رایگان و راهنمایی رایگان دارید لطفا با شماره تماسهای ذکر شده در ذیل با ما در ارتباط باشید و اگر چنانچه در این زمینه نیاز به مشاوره تخصصی و راهنمایی رایگان دارید لطفا شماره تماس خود را در فرم ذیل وارد نمایید تا همکاران ما در واحد پشتیبانی در اسرع وقت با شما در تماس باشند.
*** گردآوری و تایپینگ توسط شرکت بنیان طب جراح ***







