مبانی طب مراقبت های ویژه
مقدمه
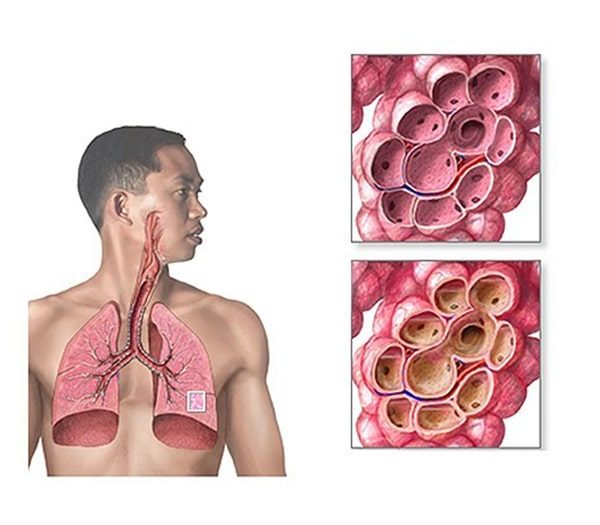
طب مراقبت های ویژه در دهههای گذشته به دلیل فن آوریهای جدید تحت دگرگونیهای شگرفی قرار گرفته است، ولی در این میان نباید نقش اطلاعات به دست آمده از کارآزماییهای بالینی که استانداردهایی را در درمان بیماران بستری در این بخش بنا نهاده اند، فراموش شود. از زمان همه گیری پولیومیلیت در دهه ۱۹۵۰، بخشهای مراقبت ویژه به روشنی نقش مفید خود را در درمان اختلالات حاد برگشت پذیر، اثبات نمودهاند. با این حال، به دلیل پیشرفت مداوم فن آوریهای مورد استفاده و نیاز به کنترل دقیق و حجم وسیع برنامه درمانی، ارائه خدمات مراقبتهای بحرانی گران است و تا ۳۰٪ کل هزینههای بیمارستانی را تشکیل میدهد.بیماران بستری در بخش مراقبت های ویژه (ICU)، جمعیتی ناهمگن هستند و طیف بیماریهای آنها از شوک سپتیک و نارسایی تنفسی تاکتواسیدوز دیابتی و خونریزی از دستگاه گوارشی فوقانی گسترده است. این فصل، در مورد چند مورد از شایعترین وضعیتهای پیش آمده در ICU که غالبا توسط متخصص ریه درمان میشوند، بحث میکند. این موارد عبارتاند از نارسایی حاد تنفسی و تهویه مکانیکی، آسیب حاد ریه و شوک.
نارسایی حاد تنفسی
وقتی ریه دیگر نمیتواند به میزان کافی به تبادل گازهای تنفسی بپردازد، نارسایی حاد تنفسی پیش میآید. این وضعیت در صورت عدم درمان، منجر به مرگ بیمار میشود. به نارسایی تنفسی همراه با عدم توانایی در اکسیژن رسانی، نارسایی تنفسی همراه با هیپوکسمی گفته میشود (نوع ۱). در صورتی که نارسایی تنفسی همراه با ناتوانی در انجام تهویه باشد، نارسایی تنفسی همراه با هیپرکاربی نامیده میشود (نوع ۲). این اختلالات، به ترتیب خود را به صورت تغییر در فشار نسبی اکسیژن شریانی (Pao۲) و فشار نسبی دی اکسیدکربن شریانی (Paco۲) شان میدهند.
نوع اول نارسایی تنفسی
در نوع ۱ نارسایی تنفسی، هیپوکسی بدون هیپرکاربی وجود دارد و به دلیل بیماریهای بینابینی ریه (مثل پنومونی، آمفیزم)، بیماریهای پارانشیم ریه ناشی از بهم خوردن جور شدن V / Q یا بیماریهای عروقی ریه مثل آمبولی ریه رخ میدهد.
نوع دوم نارسایی تنفسی
در نارسایی تنفسی نوع ۲، به دلایل متفاوتی مثل بیماری راههای هوایی، کاهش رانه تنفسی و اختلالات قفسه سینه، تهویه ناکافی است. تهویه ناکافی سبب هیپوکسی همراه با هیپرکاربی میشود.
مقادیر Pao۲ و Paco۲ که نارسایی تنفسی برحسب آنها تعریف میشود تا حدی اختیاری هستند ولی اگر در مریضی که از هوای اتاق تنفس میکند، Pao۲ کمتر از mmHg 60 یا Paco۲ بالاتر از mmHg 45 باشد، نارسایی واضح تنفسی وجود دارد. توجه به این نکته حایز اهمیت است که این مقادیر نه معادل با نیاز به تهویه مکانیکی هستند و نه شیب فشار جدیده معکوس شده از حبابچهها به راههای برطرف کننده نیاز به تهویه مکانیکی میباشند.
درمان نارسایی تنفسی
درمان نارسایی تنفسی، به تظاهرات بالینی آن بستگی دارد. بیماران مبتلا به نارسایی تنفسی که بیدارند، قادر به همکاری با پزشک میباشند و از نظر همودینامیکی وضعیت پایداری دارند، ممکن است تا زمانی که به طور مداوم تبادل گاز و وضعیت کلی آنها پایش میشود بتوانند درمان تنفسی را بدون لولهگذاری و تهویه مکانیکی تحمل نمایند. این موارد معمولاً شامل مبتلایان به بیماری انسدادی مزمن ریه (COPD) میشود که گاهی میتوانند Paco تا mmHg ۸۵ را نیز تحمل نمایند که میتواند در غیاب اسیدوز تنفسی شدید رخ دهد.
بالعکس، بیماران مبتلا به نارسایی حاد تنفسی همراه با شواهدی از زجر تنفسی شدید (برای مثال، سرعت تنفس > ۳۰ بار در دقیقه)، بدتر شدن وضعیت هشیاری (برای مثال، مختل شدن قضاوت، گیجی، توهم، خواب آلودگی) یاناپایداری همودینامیکی (برای مثال، اختلال ریتم قلب با کاهش یا افزایش تعداد ضربان ، افت فشارخون) معمولاً نیازمند لولهگذاری و تهویه مکانیکی میباشند. در موارد اخیر، صبر کردن جهت تعیین گازهای خون شریانی لازم نیست و ممکن است تعویق درمان، موجب خطراتی برای بیمار شود. اگرچه ارزیابی گازهای خون شریانی در تصمیم گیری جهت نیاز بیماران مبتلا به نارسایی تنفسی به تهویه مکانیکی بسیار مهم است، نهایتاً این وضعیت بالینی بیمار است که مسیر درمان و اقدامات پزشکی را تعیین میکند.
تهویه مکانیکی
تهویه مکانیکی عمدتاً از اصول تهویه با فشار مثبت بهره میگیرد. هوا با فشار به درون راههای هوایی مرکزی رانده شده، فشار راه هوایی مرکزی را افزایش میدهد. هواء شیب فشار از راههای هوایی مرکزی به حبابچهها را تعقیب میکند و موجب اتساع ریهها میشود. با بادشدن ریهها و متوقف شدن راندن هوا توسط دستگاه به درون راههای هوایی مرکزی، فشار داخل حبابچه ای افزایش و فشار راه هوایی مرکزی کاهش مییابد. بازدم هنگامی رخ میدهد که هوا، شیب فشار جدیدا معکوس شده از حبابچهها به راههای هوایی مرکزی را تعقیب میکند.
فواید تهویه مکانیکی
فواید عمده تهویه مکانیکی هنگام نارسایی تنفسی بهبود تبادل گاز و کاهش کار تنفس میباشند. تهویه مکانیکی با بهبود جور شدن نسبت تهویه به خونرسانی (V/Q) تبادل گازها را بهبود میبخشد. بهبود جورشدن V/Q عمدتاً به خاطر کاهش شنت فیزیولوژیک میباشد. تغییر مکانیک ریه امتلا افزایش مقاومت راههای هوایی، کاهش اتساع پذیری ریه) و افزایش تقاضای تنفسی (مثلا اسیدوز متابولیک کار تنفس را افزایش میدهند. عضلات تنفسی و دیافراگم در حین تلاش برای حفظ کار افزایش یافته تنفس میتوانند خسته شده و منجر به نارسایی تنفس گردند. تهویه مکانیکی میتواند مقداری با هم کار افزایش یافته تنفس را تقبل کرده به عضلات تنفسی اجازه رفع خستگی بدهد. در بیماران دچار نارسایی حاد تنفسی، رو به وخامت رفتن تبادل گازها که به تمهیدات محافظه کارانه پاسخ نمیدهد و زجر تنفسی، شایعترین علل تهویه مکانیکی میباشند. عوارض فوری که به دلیل تهویه مکانیکی اتفاق میافتند شامل آسیب فشاری که سب پنوموتوراکس میشود، پنوموندیاستن یا آمفیزم زیر جلدی هستند، آتروفی دیافراگم و اختلال حرکت موکوسیلیاری هم رخ میدهد.
تهویه مکانیکی غیرتهاجمی
گرچه لولهگذاری و تهویه مکانیکی معمولاً گزینههای ارجح در نارسایی تنفسی میباشند که قابل برگشت تلقی میشود در بیماران خاص تهویه غیر تهاجمی با فشار مثبت (NPPV) سودمندی خود را اثبات کرده است. NPPV به تهویه با فشار مثبت اشاره دارد که از طریق یک واسط غیر تهاجمی (ماسک بینی، ماسک صورت، یا دماغ گیر) به جای واسط تهاجمی الوله داخل نای، تراکئوستومی) به ریهها رسانده میشود. انتخاب بیماران برای تهویه غیر تهاجمی با فشار مثبت نیاز به مطرح ساختن دقیق موارد لزوم و منع انجام آن دارد. در کل NPPV در بیمارانی که دچار آدم ریوی حاد قلبی یا نارسایی تنفسی هیپرکا پنیک ناشی از COPD شده اند و نیازمند لولهگذاری فوریتی نبوده و منعی برای انجام آن ندارند ارزش آزمودن را دارد.
موارد منع انجام تهویه غیر تهاجمی با فشار مثبت شامل ایست قلبی یا تنفسی؛ ناتوانی در همکاری، حفظ راه هوایی، یا پاکسازی ترشحات؛ استفراغ غیر قابل کنترل، استفراغ خونی یا خلط خونی (هموپتزی)؛ اختلال شدید هشیاری؛ جراحی، ضربه، یا بدشکلی صورت؛ تخمین مدت زمان طولانی استفاده از تهویه مکانیکی؛ و آناستوموز اخیر مری میباشند. مواردی که در شروع نشان دهنده احتمال موفقیت تهویه هستند، اصلاح قابل توجه PH (مثل اسیدوز تنفسی) و کاهش در Paco۲ بیشتر از ۸ میلی متر جیوه هستند.
تهویه مکانیکی تهاجمی
به محض اخذ تصمیم برای لولهگذاری، یک فرد با تجربه باید به سرعت این کار را انجام دهد. عوارض لولهگذاری معمولاً مرتبط با هیپوکسمی طولانی مدت در نتیجه تأخیر در انجام لولهگذاری میباشند اما شامل استفراغ و آسپیراسیون محتویات معده، آسیب به تارهای صوتی، خونریزی، پنوموتوراکس، اختلال ریتم قلبی، و ایست قلبی نیز میشوند. به محض قرار دادن، موقعیت داخل نای باید با ارزیابی دی اکسیدکربن بازدمی تأیید شود. لوله داخل نای باید محکم شده و موقعیت آن را با معاینه صداهای تنفسی و به دنبال آن عکس قفسه سینه مورد ارزیابی قرار داد. گهگاه دید مستقیم از طریق یک برونکوسکوپ برای لولهگذاری موفق لازم است.
تنظیمات ابتدایی
تنظیمات ابتدایی دستگاه ممکن است متفاوت باشند اما به طور معمول شامل حالت دستگاه، کسر اکسیژن دمی (FIO) برابر با ۱ (یا ۱۰۰٪)، سرعت تنفس و حجم جاری هستند. کفایت تنظیمات دستگاه باید با تعیین مکرر سطح گازهای خون شریانی و ارزیابی بالینی بیمار تعیین گردد. به محض میزان کردن تنظیمات دستگاه برای حفظ سطوح نسبتاً طبیعی گازهای خون شریانی (pH 3/7 تا ۴۵/۷؛ mmHg 60 Pao۲> ؛ mmHg 45-30 Pco۲>) باید توجه به شکل دادن یک برنامه نگهدارنده معطوف گردد که اکسیژن رسانی و تهویه کافی تا درمان علت نارسایی تنفسی و در آمدن از نارسایی را تضمین کند. این برنامه باید شامل ارزیابی نیاز به آرامبخشی، راهبرد مناسب تهویه مکانیکی، تمهیدات حمایتی برای دستیابی به پایداری همودینامیک، ارزیابی وضعیت تغذیهای، و درمانهایی با هدف رفع فرایندهای آسیب رسان ابتدایی که نارسایی تنفسی را آغاز کردهاند باشد. بیشتر بیماران برای کاهش ناراحتی ناشی از تهویه مکانیکی و کاهش کار تنفس نیازمند آرام بخشی هستند اما به علت همراه بودن آن با کاهش فشار خون باید با احتیاط تجویز شود.
حالتهای مورد استفاده رایج در تهویه مکانیکیبا توجه به چه پارامتری تعیین میشوند؟
حالتهای مورد استفاده رایج در تهویه مکانیکی با طول مدت دم تعیین میشوند که میتواند بوسیله حجم، فشار، جریان، یا زمان محدود گردد. در تهویه محدود شونده با حجم، دم پس از تحویل یک حجم جاری از پیش تعیین شده متوقف میگردد. فشار مجاری هوایی طی تهویه مکانیکی محدودشونده با حجم متغیر بوده و به اتساع پذیری سیستم تنفسی، مقاومت مجاری هوایی، و مقاومت لولهها بستگی دارد. تهویه کمک-کنترل (ACV)، تهویه اجباری مداومه (CMV)، و تهویه اجباری متناوب هماهنگ (SIMV) همگی مثالهایی از حالتهای تهویه مکانیکی هستند که میتوانند با حجم محدود شوند.
CMV دارای سرعت و حجم جاری از پیش تعیین شده میباشد که اجازه تنفس خودبه خود به بیمار را نمیدهد. ناهماهنگی دستگاه و بیمار معضل بزرگی است و به همین سبب از CMV ندرتا استفاده میشود. حالت کمک-کنترل از این نظر که دارای سرعت و حجم جاری از پیش تعیین شده است شبیه CMV میباشد اما این حالت به بیمار اجازه میدهد تا تنفسهای خودبه خودی اضافهتری را نیز آغاز کند. هنگامی که دستگاه حس کند بیمار تلاش دارد که نفس بکشد حجم جاری تعیین شده را به ریهها میرساند. SIMV از این نظر که سرعت و حجم جاری از پیش تعیین شده دارد شبیه حالت کمک-کنترل میباشد. همچنین بیمار قادر است تا تنفس خود به خود آغاز کند. با این حال ممکن است این تنفس خودبه خود حجم جاری بسیار اندک داشته باشد در حالیکه مستلزم کار تنفسی قابل ملاحظهای میباشد. نتیجتاً این حالت از تهویه مکانیکی به ندرت مورد استفاده قرار میگیرد مگر هنگامی که بخواهیم بیمار را از تهویه مکانیکی جدا کنیم.
در تهویه مکانیکی به حالت کنترل فشار PCV، دستگاه تنفس هایی به بیمار میدهد که چرخه آنها براساس فشار کنترل میشود و نه حجم. در این حالت فشار مورد استفاده برای هر تنفس تعیین میگردد. هنگامی که بیمار تلاش میکند تا یک تنفس خود به خودی انجام دهد دستگاه یک تنفس با فشار تعیین شده به ریهها میرساند. این حالت ممکن است در محدود ساختن فشار راههای هوایی در بیمار مبتلا به اسپاسم برونش یا ریههای غیرارتجاعی مفید باشد زیرا خطر پنوموتوراکس (آسیب فشاری) را کاهش میدهد. چون ممکن است حجمهای جاری متفاوت باشند این حالت باید در بالین بیمار عیارسنجی شود تا تنظیمات فشاری مناسب تعیین گردد. پزشک باید دستور حداقل حجم جاری مطلوب را بدهد.
تهویه با حمایت فشار (PSV) فقط برای بیمارانی کاربرد دارد که تنفس خودبه خودی دارند. فشارهای دمی و بازدمی تعیین میشوند و تنفس اجباری از طرف دستگاه انجام نمیگیرد. از نظر بیماران این حالت از تهویه مکانیکی راحتتر است. با این حال از این حالت فقط باید در بیمارانی استفاده شود که رانه تنفسی پایدار (بدون آرامبخشی زیاد) و اتساع پذیری پایدار ریه دارند. تهویه با حمایت فشار به طور معمول در بیمارانی استفاده میشود که در حال جدا شدن از حمایت تهویه مکانیکی هستند.
کنترل حجم با تنظیمات فشار، تهویه با رهاسازی فشار راه هوایی، و تهویه با تواتر بالا روشهای جدیدتری هسند که به طور روزافزون در طبابت بالینی مورد استفاده قرار میگیرند.
تنظیمات
در هنگام آغاز تهویه مکانیکی باید تنظیمات متعددی را مدنظر قرار داد. اینها عبارتند از: حجم جاری، سرعت تنفس، حالت شروع تهویه و حساسیت، کسر اکسیژن دمی، فشار مثبت انتهای بازدمی (PEEP)، سرعت جریان، و الگوی جریان حجم جاری مناسب اولیه به عوامل متعددی بستگی دارد که قابل توجهترین آنها بیماری زمینهای است که فرد به خاطر آن نیازمند تهویه مکانیکی شده است. سپس میتوان به تدریج حجم جاری را کم یا زیاد کرد تا به pH و فشار دی اکسیدکربن شریانی (Paco۲) مطلوب دست یافت. در حالت کلی حجم جاری بالا میتواند باعث آسیب فشاری یا حجمی گردد که خطر آسیب ریوی مرتبط با دستگاه تهویه مکانیکی را افزایش میدهند. به همین سبب حجم جاری نباید بدون مد نظر قرار دادن اثرات آن روی فشار راههای هوایی یا احتمال آسیب ریوی ناشی از دستگاه تهویه مکانیکی افزایش یابد. در سندرم زجر تنفسی حاد (ARDS) حجم جاری ۶ میلی لیتر به ازای هر کیلو از وزن ایده آل با بهبود مرگ و میر همراه است (سطح ۱ شواهد).
یک روش بهینه برای تنظیم سرعت تنفس محرز نشده است. به محض تثبیت حجم جاری میتوان در حین پایش فشار مثبت انتهای بازدمی خودکاره سرعت تنفس را برای دست یافتن به pH و Paco۲ مطلوب به تدریج کم یا زیاد کرد. بیمارانی که تنفس خودبه خودی دارند در همه حالتهای تهویه مکانیکی به جز CMV سرعت تنفس خود را تنظیم میکنند. و باید از حداقل کسر اکسیژن دمی (FIO) ممکن که برای برآورده ساختن اهداف اکسیژن رسانی ضرورت دارد استفاده کرد. این کار از احتمال وقوع عواقب سوء ناشی از اکسیژن مکمل مثل آتلکتازی جذبی، تشدید هیپرکا پنه، آسیب راه هوایی، و آسیب پارانشیم ریه خواهد کاست.
عموماً فشار مثبت انتهای بازدمی (PEEP برای جلوگیری از روی هم خوابیدن حبابچهها در انتهای بازدم افزوده میشود. PEEP عموماً جور شدن تهویه خونرسانی (V/Q) و اکسیژن رسانی شریانی را بهبود بخشیده و امکان کاهش ,FI0 و نتیجتا کاهش خطر سمیت اکسیژن را فراهم میآورد. با این حال افزایش سطح فشار مثبت انتهای بازدمی تجویز شده میتواند عواقب سوء مثل کاهش پیش بار [قلب] (و کاهش برونده قلبی)، افزایش فشار کفه در راه هوایی (و افزایش خطر آسیب فشاری)، و اختلال در جریان خروجی وریدهای مغزی و افزایش فشار داخل جمجمهای داشته باشد. مقدار مطلوب PEEP، بدون پرهوایی ریه، اکسیژن رسانی را افزایش داده و فشار خون را کاهش میدهد.
متخصصان به طور معمول سرعت جریان دمی، الگوی جریان، و میزان فشار منفی لازم برای آغاز تنفس توسط دستگاه را نیز تنظیم میکنند. اگر این تنظیمات دستگاه با ملاحظه دقیق مکانیک تنفس بیمار میزان نشوند دو مشکل شایع میتواند رخ دهد. و عدم هماهنگی بیمار و دستگاه در صورتی رخ میدهد که مراحل تنفس داده شده توسط دستگاه با الگوی نفس کشیدن بیمار جور نباشد. عدم هماهنگی بیمار و دستگاه میتواند باعث تنگی نفس، افزایش کار تنفس، و طولانی شدن مدت زمان تهویه مکانیکی گردد. این مشکل با تحت نظر قرار دادن دقیق بیمار و مطالعه شکل امواج دستگاه قابل تشخیص است. عموماً ناهنجاری که به آسانی آشکار میگردد ناتوانی دستگاه در آغاز کردن یک تنفس به هنگامی است که بیمار یک تلاش تنفسی انجام میدهد.
فشار مثبت انتهای بازدمی خودکار معمولاً زمانی دیده میشود که بیمار قبل از آغاز تنفس بعدی ریههای خود را به طور کامل در حین بازدم تخلیه نمیکند. این وضعیت به عنوان انباشتگی تنفس یا ایجاد فشار مثبت انتهای بازدمی خودکار معروف است. این مشکل به ویژه در مبتلایان به حمله پایدار آسم یا تشدید بیماری انسدادی مزمن ریه (COPD) که نیازمند تهویه مکانیکی هستند نگران کننده است. فشار مثبت انتهای بازدمی خودکار در بیماران تحت تهویه مکانیکی ممکن است باعث آسیب فشاری یا شوک در اثر فشارهای بالای داخل قفسه سینه گردد که مانع بازگشت خون به بطن راست میشوند.
جدا کردن از تهویه مکانیکی
عوارض لولهگذاری داخل نای و تهویه مکانیکی کم نیستند و مهمترین آنها، آسیب فشاری، آسیب حجمی (مثل آسیب حاد ریه به دلیل حجمهای جاری بالا و پنومونی میباشند. جدا کردن از تهویه مکانیکی باید بر مبنای یک برنامه روزانه باشد. به ویژه پس از بهبودی صدمه اولیه که منجر به نارسایی تنفسی گردیده. احتمال موفقیت جدا کردن در صورت بیدار بودن و همکاری بیمار و فقدان نشانههای ناپایداری تنفسی یا همودینامیک بیشتر است. معمولاً در صورت تداوم نیاز به اکسیژن کمکی زیاد (۰۵ <FIO۲)، تلاش برای جدا کردن از تهویه مکانیکی صورت نمیگیرد.
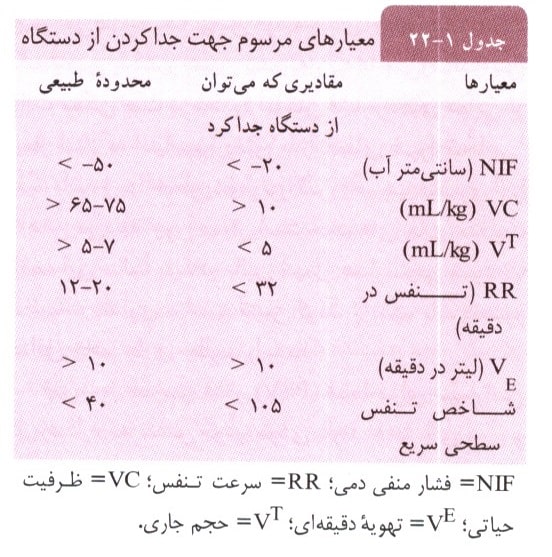
معیارهای مرسوم که تعیین کننده امکان قطع تهویه مکانیکی هستند، عبارتاند از فشار منفی دمی، ظرفیت حیاتی، حجم جاری، سرعت تنفس و تهویه در دقیقه (جدول ۱-۲۲). متأسفانه، قدرت این معیارها در پیشگویی کردن عدم امکان قطع تهویه مکانیکی هستند و نمیتوانند برقراری موفقیت آمیز تنفس خودبه خودی را پیش بینی نمایند. یک راه بهتر جهت ارزیابی توانایی قطع تهویه، قرار دادن بیمار در یک قطع آزمایشی تهویه به مدت کوتاه است که در طی آن حمایت دستگاه کاهش مییابد. یک راهبرد دیگر، کاهش فشار تولید شده توسط دستگاه تهویه گر در طی دورهای از فشار مثبت مداوم مجاری هوایی (CPAP) به صورت آزمایشی است. بیمار از نظر وجود هرگونه نشانهای از زجر تنفسی یا ناپایداری همودینامیک پایش میشود و سطح گازهای خون شریانی جهت تعیین مؤثر بودن تهویه خود به خودی، اندازهگیری میگردد. اگر بیمار بتواند این دوره آزمایشی را تحمل نماید، ممکن است بسته به وضعیت بالینی بیمار و بیماری زمینهای وی، بتوان لوله را خارج نمود.
اصطلاحات پزشکی
اگرقطع آزمایشی تهویه شکست بخورد باید تلاشهایی جهت شناسایی عوامل مسؤل صورت گیرد. در افراد شدید بیمار ممکن است همه عوامل دخیل آشکار شناسایی و تصحیح شده باشند اما بیمار قبل از خارج ساختن لوله داخل نای همچنان نیازمند جداساختن آزمایشی طولانیتر باشد. دو راهبرد برای جداساختن بیمار از تهویه مکانیکی در این زمینه توصیه شده است. اولی درگیر کردن بیمار در تهویه خود به خودی آزمایشی بدون فشار مثبت برای ۱ ساعت یک یا دو بار در روز همراه با حمایت تهویهای کامل بین هر دوره و معمولاً از طریق تهویه کمک-کنترل یا کنترل فشار میباشد. میتوان طول مدت تنفس خودبه خود آزمایشی را به تدریج بیشتر کرد تا جاییکه دیگر بیمار نیازی به حمایت تهویه مکانیکی نداشته باشد. راهبرد دیگر از تهویه با حمایت فشار بهره میبرد. فشار دمی رفته رفته کاهش داده میشود تا بیمار بتواند بدون حمایت دستگاه به طور خودبه خود نفس بکشد.
به نظر میرسد هر دو راهبرد به یک اندازه کارآیی داشته باشند گرچه جدا کردن از دستگاه از طریق تهویه با حمایت فشار در مبتلایان به بیماری مزمن ریوی که به مدتهای طولانی تحت تهویه مکانیکی قرار داشته اند ممکن است ارجحیت داشته باشد. مطالعات نشان داده است در بیمارانی که به مدت طولانی تهویه مکانیکی داشته اند، انجام تراکئوستومی اولیه برای جدا ساختن از دستگاه مفید است و به دلیل اینکه به راحتی و مکرر میتواند برداشته شود، تنفس خود به خودی آزمایشی و بدون حمایت دستگاه را تسهیل میکند (سطح ۲-۱ شواهد).
آسیب حاد ریه
به وخیمترین نوع آسیب حاد و منتشر ریه، سندرم زجر تنفسی حاد (ARDS) گفته میشود که معمولاً با تنگی نفس، سیانوز، تا کی پنه، تاکیکاردی، تعریق و رال منتشر در معاینه خود را نشان میدهد. مشخصه آسیب حاد ریه افزایش نفوذ پذیری غشای حبابچهای-مویرگی است که منجر به پرشدن فضای حبابچهای از مایع حاوی ماده پروتئینی میشود. ARDS از طریق معیارهای بالینی شدت اختلال عملکرد ریه تعریف میشود (برای مثال، Pao۲/FIO2 ).
تعریف جدید ARDS
بر اساس تعریف جدید ARDS در برلین در سال ۲۰۱۲ شدت ARDS به انواع خفیف، متوسط و شدید تقسیم میشود. ARDS خفیف در تنظیمات تهویه مکانیکی نیاز به نسبت Pao۲/FIO۲ ۲۰۰ تا ۳۰۰ میلی متر جیوه دارد (PEEP یا CPAP 5 سانتی متر آب). ARDS متوسط یا شدید زمانی اتفاق میافتد که در تنظیماتPao۲/FIO۲ بین ۱۰۰ و ۲۰۰ میلی متر جیوه یا کمتر باشد (PEEP با CPAP 5 سانتی متر آب). نارسایی تنفسی نباید به دلیل نارسایی قلبی یا احتباس مایع باشد؛ کدورتهای دو طرفه دال بر ادم ریوی باید روی عکس ساده قفسه سینه یا CT وجود داشته باشد؛ علایم تنفسی شروع ناگهانی باید داشته و به دلیل یک آسیب بالینی مشخص (کمتر از یک هفته اتفاق افتاده باشد. معیارهای دیگر رد کردن ادم ریوی قلبی و سایر علل نارسایی تنفسی هیپوکسمیک حاد مثل فیبروز ریوی ایدیوپاتیک بیماری بینابینی مزمن ریه و خونریزی حبابچهای منتشر هستند
این فرایند، توسط وارد آمدن آسیب مستقیم به ریه مثل پنومونی آسپیراسیون، استنشاق دود و غرق شدگی تقریبی یا آسیب سیستمیک مانند ضربه، جراحی، سپسیس سوختگیها، شکستگی استخوانهای دراز، پانکراتیت اور می، تزریق خون، شوک، مسمومیت دارویی بابای پس قلبی ریوی ایجاد میشود. هر سال تقریباً ۱۵۰.۰۰۰ مورد ARDS در ایالات متحده گزارش میشوند و پنومونی آسپیراسیون و سپسیس، شایعترین بیماری همراه هستند. میزان مرگ و میر ناشی از ARDS زیاد است و تقریباً ۵۰-۳۰% بیماران میمیرند.
ARDS دقیقا چیست؟
ARDS، تظاهر ریوی یک اختلال سیستمیک است که به نظر میرسد موجب شروع یک پاسخ التهابی خارج از قاعده به آسیب میشود. التهاب کنترل نشده، موجب آسیب به اندوتلیوم و اپیتلیوم عروق ریه میشود که به نوبه خود نفوذپذیری این دو سطح فیزیولوژیک را بالا میبرد و منجر به خروج مایع ادم پروتئین دار از فضای داخل عروقی و تجمع آن در بافت بینابینی ریه و فضاهای حبابچهای میشود. آسیب به اپیتلیوم ریه منجر به کاهش جذب آب از فضای حبابچهای میگردد و سب ترشح مقادیر غیر طبیعی یا ناکافی سورفاکتانت میشود.
به ARDS معمولاً خیز ریوی غیرکاردیوژنیک یاخیز ریوی ناشی از افزایش نفوذپذیری گفته میشود. این فرایندها در ریه موجب شنت داخل ریوی راست به چپ میشوند که منجر به هیپوکسمی مقاوم و کاهش اتساع پذیری ریوی و در نتیجه، افزایش کار تنفس میشوند عکس سینه ارتشاح حبابچهای منتشر دوطرفه را نشان میدهد. نارسایی اندامهای دیگر و در نتیجه، نارسایی چند اندام به طور همزمان به خصوص در زمینه سپسیس شایع است.
مشخصه ARDS از نظر بافت شناختی، آسیب منتشر حبابچه ای همراه با غشاهای هیالینی است. کاهش کمیت و کیفیت سورفاکتانت ساخته شده، بر شدت ضایعه میافزاید و منجر به آتلکتازی میشود. پس از چند روز، بررسی بافت نشان دهنده هیپرپلازی پنوموسیتهای نوع II و رسوب بافت همبند است که منجر به فیبروز میشود. این وقایع ممکن است در اثر تهویه مکانیکی با فشار مثبت، اتساع بیش از حد قفسه سینه و بیش بود اکسیژن تشدید شوند.
باید در بیماران دارای شرایط مستعدکننده (مانند سپسیس)، ارتشاح دوطرفه ریه در عکس سینه و هیپوکسمی مقاوم (یعنی نسبت Pao۲ به FIO۲ برابر mmHg 200 یا کمتر) و در غیاب اختلال عملکرد قابل توجه قلبی، تشخیص ARDS را مد نظر قرار داد. در حال حاضر، درمان ARDS بر روشهای حمایتی معطوف به ریشه کن کردن عامل آسیب رسان، حفظ سیستم قلبی- عروقی، فراهم کردن تغذیه و جلوگیری از افزایش بار حجمی مایع متکی است. کار آزمایی مایع درمانی و کاتتر (FACCT) که توسط مجمع بین المللی خون، ریه و قلب انجام شد، نشان داد که در راهبرد مایع درمانی محافظه کارانه نسبت به راهبرد رادیکال تره روزهای بدون تهویه مکانیکی (۵/۲ روز) و بدون ICU ( (2/2روز بیشتری وجود دارد (سطح ۱ شواهد). روش تهویه مکانیکی که حجم جاری که به کار میبرد (حدود ۶ میلی لیتر به ازای هر کیلوگرم از وزن بدن) بقاء را افزایش میدهد سطح ۱).
پیشرفتهایی که در اکسیژن رسانی غشایی خارج تنهایی (ECMO ) و PECLA گزارش شده، نارساییهای قبلی این ابزارها را در بیماران با آسیب حاد ریه زیر سؤال میبرد. کارآزمایی CESAR تهویه مکانیکی معمول را با ECMO در موارد نارسایی شدید تنفسی مقایسه کرد و نشان داد که بیمارانی که تحت ECMO قرار میگیرند بهبود قابل توجهی در بقاء همراه با کاهش ناتوانی در مدت ۶ ماه دارند سطح ۱ شواهد). ECMO میزان مرگ و میر را در بیماران جوانتر مبتلا به ARDS ناشی از HIN1 بهبود بخشید (سطح II-2). چندین کارآزمایی بالینی مشاهدهای و کنترل نشده هم مواردی از افزایش بقاء را نشان دادند. اما همولیز و عوارض انعقادی استفاده از ECMO را محدود کرده است.
تهویه نوسانی با تواتر بالا (HFVO) هم در بیماران با ARDs متوسط تا شدید امتحان شده است اما مرگ ومیر کاهش نداشت و در مقایسه با تهویه با فشار مثبت، نتایج بدتری داشت. سودمندی کورتیکواستروییدهاء سورفاکتانت و اکسیژن رسانی خارج بدنی اثبات نشده است و توصیه نمیشود میتوان توسط PEEP و تنفس در حالت دمروء اکسیژن رسانی را بهبود بخشید ولی به نظر نمیرسد این مداخلات بر سیر طبیعی بیماری تأثیری داشته باشند، در مقایسه تغذیه تروفیک اولیه و تغذیه رودهای کامل، میزان مرگ و میر ۶۰ روزه با روزهای بدون تهویه مکانیکی تفاوتی نداشت (کار آزمایی EDEN، سطح ۱ شواهد). بین تغذیه رودهای زودهنگام و با تأخیر هم از نظر مرگ و میر تفاوتی وجود نداشت، آنتی اکسیدانها، اسیدهای چرب امگا۳- و اسید گاما- لینولئیک سبب بهبودی در بیماران مبتلا به آسیب حاد ریه نشدند. چون هیچ درمانی که اسیب ریوی حاد را کاهش داده یا ترمیم را سرعت بخشد در دسترس نمیباشد کلید مراقبت از بیماران دچار ARDS درمان دقیق حمایتی و اجتناب از عوارضی مثل پنومونی مرتبط با دستگاه تهویه با سپسیس مرتبط با کاتتر میباشد.
نمره پیشگویی آسیب ریه (LIPS) یک ابزار غربالگری مفید در کار آزماییهای بالینی است (شواهد سطح A) که شامل وضعیتهای مساعدکننده و تعدیل کنده خطر است ارزش پیشگویی منفی ۹۷/۰–). این معیار پیش آگهی سبب میشود در زمان پذیرش بیمارانی که در معرض خطر آسیب حاد ریه یا ARDS هستند، مداخلاتی انجام شود که جلوی پیشرفت بیماری را بگیرد یا سبب پیگیری دقیق بیمار از نزدیک شود
اغلب بیمارانی که از ARDS جان سالم به در میبرند، اختلال ریوی قابل توجهی در عرض ۱۲ ماه ندارند. شایعترین عارضه دراز مدت در این بیماران، عوارض عصبیعضلانی و روانی- اجتماعی است (سطح A شواهد).
شوک
شوک به صورت کاهش خونرسانی عمومی به اندامها، معمولاً همراه با کاهش فشار خون تعریف میشود و منجر به آسیب یا مرگ سلولها میشود.
شوک به چهار دسته تقسیم میشود:
(۱) شوک قلبی (کاهش برونده قلبی به دلیل اختلال عملکرد قلب)
(۲) شوک ناشی از کاهش حجم (کاهش حجم داخل عروقی)
(۳) شوک سپتیک با شوک ناشی از توزیع مجدد (کاهش مقاومت عروق سیستمیک)
(۴) شوک انسدادی (کاهش برونده قلبی به دلیل انسداد در مسیر جریان خون).
در مواجهه با بیمار دچار شوک، باید سریعا از وی رگ گرفته شود و همزمان با ارزیابی دقیق از وضعیت، حجم زیادی از مایع به وی داده شود. این راهبرد، به خصوص زمانی مفید است که تصور میشود علت شوک، کمبود حجم یا سپسیس باشد. در مورد شوک قلبی، برنامه درمانی به گونهای طرح ریزی میشود که عملکرد قلب بهبود یابد. در این موارد، از تجویز داروهای افزاینده توان قلب و در موارد شدید و مقاوم، از بای پس قلبی یا وسایل کمکی قلب استفاده میشود. در کاهش شدید حجم، معمولاً تجویز سالین کافی است. در سپسیس، جایگزینی مایع، درمان آنتی بیوتیکی و تخلیه هر فضای حاوی عفونت الزامی است.
شوک انسدادی چه زمانی رخ می دهد؟
شوک انسدادی که نتیجه انسداد در مسیر جریان خون است، در آمبولی حجیم ریوی یا آمبولی زین اسبی که در محل دوشاخه شدن شریانهای ریوی راست و چپ جایگزین میشود، به وجود میآید. در این موارد، رفع انسداد از طریق مکانیکی یا روشهای دیگر (مانند ترومبولیز) یا حمایت کردن از گردش خون بیمار تا زمان برطرف شدن انسداد، مهم است.
در درمان شوک، پایش فشارخون و خون رسانی به اندامها، اهمیتی غیرقابل انکار دارد. تجویز مایعات از طریق یک ورید مرکزی راحتتر است و از طریق شریان میتوان به طور صحیح، فشار خون را پایش نمود. اگرچه قرار دادن یک کاتتر در شریان ریوی (Swan- Ganz) در کارآزماییهای اولیه نتایج خوبی برای گروه خاصی از بیماران داشت، اما مطالعات اخیر آن را مفید نمیدانند (مانند مطالعه FACTT سطح ۱ شواهد). این کاتتر، امکان سنجش مستقیم فشار دهلیز راست، بطن راست، شریان ریوی و فشار گوهای مویرگهای ریه و اندازهگیری برونده قلبی را فراهم میکند.
نگرانیها در مورد سودمندی حقیقی و نسبت فایده – خطر همراه با گذاشتن این کاتتر افزایش یافته است. ثابت شده است که کاتتر شریان ریوی عوارضی مثل دیس ریتمی قلبی غیر کشنده را افزایش میدهد و در مواقع عدم پاسخ به مایع در سپسیس یک پیشگویی کننده ضعیف است. اشباع اکسیژن وریدی مرکزی (Scvco) که با کاتتر وریدی مرکزی اندازهگیری میشود، مشابه اشباع اکسیژن وریدی مخلوط ۱ (Swo) است. قرار دادن این کاتترها و تفسیر صحیح دادههای جمع آوری شده، نیازمند تخصص قابل توجه است.
سندرم پاسخ التهابی
سیستمیک سندرم پاسخ التهابی سیستمیک (SIRS)، مجموعهای از نشانهها و علائم بالینی است که در اثر پاسخ میزبان به صدمات مختلف آغاز میگردد. شایعترین علت SIRS عفونت است که به آن سپسیس گفته میشود. با این حال، پدید آمدن SIRS توسط اختلالات غیرعفونی مانند پانکراتیت و مسمومیت دارویی، ناشایع نیست.
تشخیص SIRS نیازمند وجود حداقل دو تا از ملاکهای ذیل است:
(۱) دمای بدن بالاتر از C°۳۸ یا کمتر از C° ۳۶.
(۲) ضربان قلب بیشتر از ۹۰ ضربه در دقیقه.
(۳) تا کی پنه بیشتر از ۲۰ تنفس در دقیقه.
(۴) ,Paco کمتر از mmHg ۳۲.
(۵) شمارش گویچه سفید بیشتر از ۱۲.۰۰۰ یا کمتر از ۴۰۰۰.
این پاسخ سیستمیک، ممکن است منجر به اختلال عملکرد بسیاری از اندامها از جمله ریه، کبد، کلیهها، قلب و دستگاه عصبی مرکزی شود. به این وضعیت، سندرم اختلال عملکرد چند عضویه یا نارسایی چند عضوی گفته میشود هرچند تعداد عضوهای درگیر بیشتر باشد، پیشآگهی بدتر میشود و میزان مرگ و میر از ۳۰٪ در موارد با شدت کمتر تا بیش از ۹۰% در نارسایی پنج یا تعداد بیشتری از اندامها، متغیر است. درمان شامل احیاء سریع با مایعات یا تنگ کنندههای عروقی برای بهبود فشار خون و تجویز فوری آنتی بیوتیک پس از گرفتن کشت خون و سایر کشتها است.
بخارات و گازهای زیان آور و استنشاق دود
استنشاق بعضی گازها و بخارات خاص، ممکن است موجب خفگی یا آسیب سلولی و متابولیک شود (جدول ۲- ۲۲). مسمومیت با منواکسیدکربن، یک علت شایع آسیب استنشاقی است که به کرات مورد غفلت قرار میگیرد و از طریق جدا کردن رقابتی اکسیژن از هموگلوبین، موجب هیپوکسی بافتی میشود. تمایل منواکسیدکربن به هموگلوبین، تقریباً ۲۵۰ برابر اکسیژن است.
ارتباط بین سطح منواکسید کربن و علایم، ضعیف است ولی عموماً بیماران با سطح منواکسیدکربن بالاتر از ۳۰٪، دارای علامتاند. علائم ممکن است از گیجی و منگی یا ضعف تا تهوع، سردرد، تاکیکاردی و اغمای عمیق متغیر باشند. اساس تشخیص، زمینههای بالینی بیمار است و یافتههای آزمایشگاهی آن را حمایت میکنند. مسمومیت با منواکسیدکربن ممکن است در اتوموبیلهای دربسته، استفاده از رنگ برهایی که پایه کلرید متیلن دارند و قرار گرفتن در معرض بخاریهای نفت سوز یا آتشهای ذغال در فضاهای بدون تهویه به وجود آید.
در موارد مشکوک باید گازهای خون شریانی همراه با اشباع هموگلوبین – اکسیژن اندازهگیری (و نه محاسبه شود. باید سطح منواکسید کربن در بیماران با اشباع اکسیژن شریانی سیستمیک (Sao۲) کمتر از Sao۲ محاسبه شده از طریق فشار اکسیژن شریانی، اندازهگیری شود. درمان، شامل تنفس اکسیژن صددرصد میباشد. ممکن است اکسیژن پرفشار مفید باشد ولی این درمان ممکن به راحتی در دسترس نباشد.
استنشاق مواد سوزاننده ممکن است منجر به چه آسیب هایی شود؟
استنشاق مواد سوزاننده مانند آمونیاک، کلر و فلورید هیدروژن، موجب علائم حاد التهاب چشم و مجاری هوایی فوقانی میشود. درد، اشک ریزش، آبریزش بینی، و علائم مجاری هوایی فوقانی معمولاً فرد را وادار به ترک محیط میکنند. استنشاق دی اکسید نیتروژن (بیماری کارگران سیلو) هنگامی اتفاق میافتد که تخمیر غلات موجب تولید مقادیر زیاد این گاز میشود. اکثر بیماران بدون بر جاماندن عوارض دائمی بهبود مییابند، اما تعداد کمی از آنها ممکن است دچار برونشیولیت انسدادی (انسداد غیر قابل برگشت راههای هوایی کوچک) شوند.
تب بخار فلزات به دلیل استنشاق اکسیدهای فلز که بر اثر جوشکاری تولید میشوند، موجب پیدایش علائم شبه آنفلوانزا میشود. استنشاق پلاتین، فرمالین و ایزوسیاناتها ممکن است آسم را تشدید کند. استنشاق غلظتهای بالایی از بخارهای کادمیوم و جیوه ممکن است موجب ایجاد پنومونیت گردد.
استنشاق دود ممکن است منجر به چه آسیب هایی شود؟
استنشاق دود ممکن است منجر به آسیب گرمایی مستقیم شود که معمولاً محدود به مجاری هوایی فوقانی است ولی در صورتی که مواجهه با مقادیر کافی بخار در نتیجه محتوای گرمایی بالای آب صورت گیرد ممکن است باعث ایجاد آسیب مجاری هوایی تحتانی نیز بشود. ادم حنجره، التهاب مجاری هوایی و تولید موکوس ممکن است منجر به انسداد مجاری هوایی شوند که نیازمند لولهگذاری داخل نای میباشد. در نتیجه مصرف اکسیژن توسط آتش و نیز آسیب سیتوتوکسیک ناشی از گازهایی مانند منواکسیدکربن، سیانید و اکسیدانهایی که در طی احتراق آزاد میشوند، آنوکسی رخ میدهد. احتراق پلیمرهای طبیعی و صناعی، اغلب موجب تولید آلدئیدها، استالدئید و اکرولئین میشود که قابلیت تحریکی زیادی دارند. مسمومیت با سیانید با اتصال به سیتوکروم a۳ و a (مثل سیتوکروم c اکسیداز اکسیژن را از تولید انرژی جدا میکند، مانع از انتقال الکترون به اکسیژن میشود و نیازمند درمان سریع با اکسیژن ۱۰۰٪ و تیوسولفات سدیم است. تیوسولفات سدیم، تبدیل سیانید به تیوسیانات را تسهیل میکند. اخیره سازمان غذا و داروی ایالات متحده استفاده از هیدروکسیکوبالامین را که باسیانید برای تشکیل سیانوکوبالامین (ویتامین B۱۲)، ترکیب میشود نیز تأکید کرده است.

درمان بیماران دچار آسیبهای استنشاقی عبارت است از مراقبتهای حمایتی همراه با توجه دقیق به مجاری هوایی. باید به بیمار اکسیژن رسانده شود و پایش مداوم وضعیت قلبی و همودینامیک لازم است. گاهی برطرف کردن انسداد مجاری هوایی و جلوگیری از پیدایش نارسایی تنفسی، نیازمند لولهگذاری و تهویه مکانیکی است.
منابع
Acute Respiratory Distress Syndrome Network: Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome, N Engl J Med 342:1301-1308, 2000.
ARDS Definition Task Force, Ranieri VM, Rubenfeld GD, et al: Acute respiratory distress syndrome: the Berlin definition, JAMA 307:2526-2533, 2012.
Bernard GR, Sopko G, Cerra F, et al: Pulinonary artery catheterization and clinical outcomes: National Heart, Lung, and Blood Institute and Food and Drug Administration Workshop Report. Consensus statement, JAMA 283(19) :2568-2572, 2000.
Dellinger RP, Levy MM, Rhodes A, et al: Surviving sepsis campaign: international guidelines for management of severe sepsis and septic shock: 2012, Crit Care Med 41:580-637, 2013.
Ferguson ND, Cook DJ, Guyatt GH, et al: High-frequency oscillation in early acute respiratory distress syndrome, N Engl J Med 368:795-805, 2013.
Gajic O, Dabbagh O, Park PK, et al: Early identification of patients at risk of acute lung injury: evaluation of lung injury prediction score in a multicenter cohort study, Am J Respir Crit Care Med 183:462-470, 2011.
Griffiths J, Barber VS, Morgan L, et al: Systematic review and meta-analysis of studies of the timing of tracheostomy in adult patients undergoing artificial ventilation, BMJ 330:1243, 2005.
Hill NS: Noninvasive ventilation for chronic obstructive pulmonary discase, Respir Care 49:87-89, 2004. National Heart, Lung, and Blood Institute Acute Respiratory Distress Syndrome (ARDS) Clinical Trials Network, Wheeler AP, Bernard GR, et al: Pulmonary. artery versus central venous catheter to guide treatment of acute lung injury, N Engl J Med 354:2213-2224, 2006.
National Heart, Lung, and Blood Institute Acute Respiratory Distress Syndrome (ARDS) Clinical Trials Network, Wiedemann HP, Wheeler AP, et al: Comparison of two fluid-management strategies in acute lung injury, N Engl J Med 354:25642575, 2006.
Peek G), Mugford M, Tiruvoipati R, et al: Efficacy and economic assessment of conventional ventilatory support versus extracorporeal membrane oxygenation for severe adult respiratory failure (CESAR): a multicentre randomized controlled trial, Lancet 374:1351-1363, 2009.
Pham T, Combes A, Rozé H, et al: Extracorporeal membrane oxygenation for pandemic influenza a (HINI)-induced acute respiratory distress syndrome: a cohort study and propensity matched analysis, Am J Respir Crit Care Med 187:276-285, 2013.
Rivers E, Nguyen B, Havstad S, et al: Early goal-directed therapy in the treatment of severe sepsis and septic shock, N Engl J Med 345:1368-1377, 2001.
Sehti JM, Siegel MD: Mechanical ventilation in chronic obstructive pulmonary disease, Clin Chest Med 21:799-818, 2000. Ware LB, Matthay MA: The acute respiratory distress syndrome, N Engl J Med 342:1334-1349, 2000,

مشاوره : اگر نیاز به مشاوره رایگان و راهنمایی رایگان دارید لطفا با شماره تماسهای ذکر شده در ذیل با ما در ارتباط باشید و اگر چنانچه در این زمینه نیاز به مشاوره تخصصی و راهنمایی رایگان دارید لطفا شماره تماس خود را در فرم ذیل وارد نمایید تا همکاران ما در واحد پشتیبانی در اسرع وقت با شما در تماس باشند.
*** گردآوری و تایپینگ توسط شرکت بنیان طب جراح ***








