بیماری های انسدادی ریه (قسمت ۲)
مقدمه
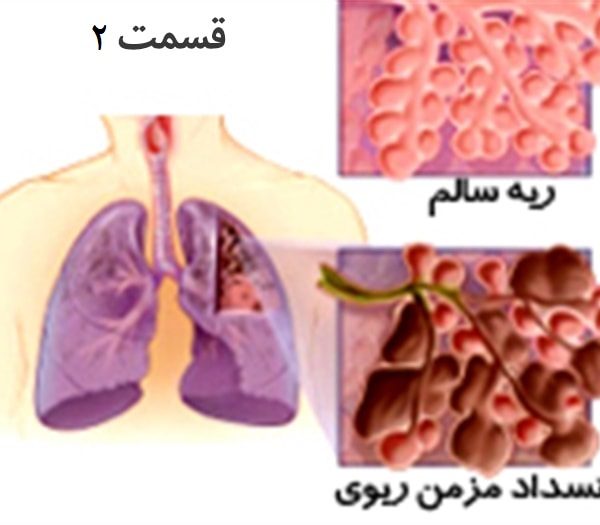
بیماری های انسدادی ریه گروهی شایع از اختلالات ریوی هستند که باعث تنگی نفس با مشخصه ی الگوی انسدادی محدودیت جریان هوای بازدمی در اسپیرومتری می شوند. این اختلالات در بر گیرنده بیماری انسدادی مزمن ریه(COPD)، آسم، فیبروز کیستیک (CF)، برونشکتازی، و بیماری های برونشیولی می باشند.
در بعضی موارد این اختلالات از نظر بالینی با هم هم پوشانی دارند و گذشته از محدودیت جریان هوای بازدمی، خصوصیات مشترکی دارند. این خصوصیات شامل علایم خس خس و تولید التهاب مزمن راه های هوایی مرکزی، وجود تغییرات ساختمانی در راه هوایی که سبب سازمان دهی مجدد(remodeling) راه های هوایی و حملات تشدید موقتی وضعیت بالینی ( exacerbation ) می شود. اما علل بیماری ها، محل درگیری و الگوی تغییرات التهابی و سازماندهی مجدد و همچنین درمان ها ، پیش آگهی ها و سیر طبیعی بیماری ها اغلب تفاوت های واضحی دارند که سبب می شود افتراق بالینی این بیماری ها از هم مهم باشد.
برونشکتازی
تعریف و اپیدمیولوژی
برونشکتازی، گشادی غیر طبیعی برونش هاست (راههای هوایی بزرگ که دیواره آن حاوی غضروف است که در اثر التهاب و تغییرات تخریبی پایدار در دیواره برونشها حادث میگردد. میزان بروز برونشکتازی نامعلوم است، اما احتمالاً بیش از ۱۰۰ هزار نفر را در ایالات متحده درگیر میکند، و بیماری در میان سالمندان شایعتر است. احتمالاً میزان بروز برونشکتازی در کشورهای در حال توسعه بالاتر است. در این مناطق پوشش واکسیناسیون کودکان کمتر و شیوع سل ریوی بیشتر است.

پاتولوژی
برونشکتازی ممکن است محدود به قسمتی از برونش یا لوب ریه بوده یا منتشر باشد، برونشهای درگیر اتساع غیر طبیعی دارند و در دیواره آنها التهاب مزمن و در فضای داخلشان التهاب نوتروفیلی همراه با عفونت و کلونیزه شدن باکتریها وجود دارد. التهاب در برونشکتازی با تغییرات ساختمانی در دیواره برونشهای مثل تخریب الیاف ارتجاعی، عضله صاف و غضروف همراه است.
مانند COPD درگیری راههای هوایی کوچک هم وجود دارد. انسداد راههای هوایی کوچک سبب افزایش مقاومت در برابر جریان هوا میشود که این امر علیرغم اتساع راههای هوایی بزرگ منجر به انسداد جریان هوا میشود. برونشکتازی از نظر پاتولوژی شامل این انواع است: توبولی یا ریز لولهای (شایعترین نوع که در آن اتساع صاف برونشها وجود دارد)، واریسی (برونشهای متسع همراه با دندانه دندانه شدن جدار به دلیل وریدهای واریسی) و کیستیک (مرحله پایانی برونشکتازی با برونشهای متسعی که به کسیههایی شبیه خوشههای انگور ختم میشوند).
در برونشکتازی این فرضیه مطرح است که یک عامل محیطی منجر به آسیب برونشها در یک فرد مستعد میشود. این امر به ترتیب سبب اختلال در پاکسازی عفونت، کلونیزه شدن باکتری و عفونت یا عفونت مجدد، وجود التهاب در راههای هوایی و آسیب بیشتر برونش و به این ترتیب یک سیکل معیوب میشود. گمان میشود یک عفونت تحریک کننده که گاهی در کودکی رخ میدهد، روند آسیب برونشها که منجر به برونشکتازی میشود را در بسیاری از موارد آغاز میکند (برونشکتازی پس از عفونت). این عفونت ممکن است یک عفونت ویروسی (مثل سرخک)، یک پنومونی نکروزدهنده (مثل پنومونی ناشی از استاف اورئوس)، سل یا عفونت با مایکوباکتریومهای غیر معمول مثل مایکوباکتریوم آویوم اینتراسلولار) باشد. چون عفونتهایی مثل مایکوباکتریوم أو یوم اینتراسلولار میتوانند سیر برونشکتازی را کمپلیکه هم بکنند، تعیین اینکه آیا عفونت مایکوباکتریوم آغازگر روند برونشکتازی است یا پیامد آن، مشکل است.
برونشکتازی موضعی چگونه عارض می شود؟
برونشکتازی موضعی ممکن است در اثر انسداد آناتومیکی ناشی از یک جسم خارجی داخل برونش، تومور، سنگ برونشی، یا به علت فشردگی از خارج ناشی از بزرگی گرههای لنفی عارض شود. سندرم لوب میانی راست در اثر باریک شدگی سوراخ برونشی لوب میانی راست اغلب توسط بزرگ شدن گرههای لنفی در جریان سل ایجاد میگردد و منجر به برونشکتازی موضعی دیستال به محل انسداد میگردد. انسداد آناتومیک منجر به عفونت مزمن یا راجعه و التهاب میگردد که در طول زمان به تغییر شکل و تخریب برونش منتهی میشود.
برونشکتازی و سیستم دفاعی
برونشکتازی منتشر میتواند ناشی از اختلالات گوناگونی در سیستم دفاعی میزبان باشد که سبب حساسیت به عفونتهای مزمن یا راجعه ریه و در نتیجه آسیب برونشها شوند. مثلاً برونشکتازی ممکن است در نقایص مادرزادی که سبب اختلال در پاکسازی راههای هوایی از موکوس میشوند، رخ دهد، مثل فیبروز کیستیک (قبلاً توضیح داده شد) یا اختلال تحرک اولیه مژکها که یک ناهنجاری ارثی نادر میکروتوبول مژک هاست. سه گانه کلاسیک سینوزیت، جابجایی احشا و ناباروری برای سندرم کار تاژنر تشخیصی است؛ این سندرم یک نوع اختلال تحرک اولیه مژکها میباشد. وضعیتهای نقص ایمنی، مانند کمبود گاماگلبولین در نقص ایمنی متغیر ترکیبی (CVID) نیز ممکن است سبب برونشکتازی شوند. کمبود آنتیتریپسین که سبب نقص فعالیت آنتی پروتئاز در ریه میشود نیز با برونشکتازی همراه است. برونشکتازی همچنین با بیماریهای بافت همبند از جمله آرتریت روماتویید نیز مرتبط میباشد.
سرانجام، برونشکتازی با شایعترین بیماری های انسدادی ریه، COPD و آسم، همپوشانی دارد. بعضی از بیماران مبتلا به COPD، برونشکتازی هم دارند، که اغلب در لوبهای تحتانی است. آسپرژیلوز برونشی- ریوی حساسیتی وضعیتی است که در بیماران مبتلا به آسمی که افزایش حساسیت به قارچهای آسپرژیلوس دارند، رخ میدهد و با برونشکتازی مرکزی، سطوح بالای ایمونوگلبولین (Ige) E و آنتی بادیهای رسوب دهنده برای گونههای آسپرژیلوس تظاهر مییابد.
تظاهرات بالینی
بیماران مبتلا به برونشکتازی با سرفه مزمن و خلط زیاد و گاهی بدبو تظاهر مییابند. حجم خلط و میزان چرکی بودن آن بیشتر از COPD یا آسم است. ممکن است تنگی نفس و خستگی هم وجود داشته باشد. خلط دارای رگههای خون شایع بوده و ممکن است خلط خونی حجیم رخ دهد. ممکن است رالهای موضعی و چماقی شدن انگشتان وجود داشته باشد، تشدیدهای دورهای ناشی از عفونت با عوامل بیماری زای باکتریایی از جمله هموفیلوس آنفلوانزا و پسودومونا آیروژینوزا شایع است. ممکن است کلونیزه شدن مایکوباکتریوم غیر سلی یا عفونت با آن هم اتفاق بیفتد. آزمونهای عملکرد ریوی ممکن است نشان دهنده انسداد خفیف تا متوسط باشند. معمولاً شواهدی به نفع پاسخدهی بیش از حد برونشها دیده نمیشود.
تشخیص و تشخیص افتراقی
ممکن است عکس سینه طبیعی بوده یا افزایش خطوط بینابینی را نشان دهد. یافته کلاسیک عبارت است از خطوط موازی در محیط ریه که به شکل ریل قطار توصیف میشوند و حاکی از دیوارههای ضخیم شده برونش میباشند که از پروگزیمال به دیستال باریک نمیشوند. HRCT برای شناسایی راههای هوایی گشاد شده حساستر بوده و در تشخیص برونشکتازی مشکوک مطالعه انتخابی است.
علایم حاکی از برونشکتازی در HRCT عبارتاند از فقدان باریک شدن تدریجی راههای هوایی در محیط ریه و وجود راههای هوایی که قطرشان از عروق مجاور بیشتر است و نیز وجود برونشهای قابل رویت در محیط ریه، ممکن است برونکوسکوپی در برونشکتازی موضعی برای ارزیابی ناهنجاریهای داخل برونش یا جسم خارجی ضرورت یابد میتوان خلط را جهت بررسی از نظر قارچ یا مایکوباکتریوم که ممکن است عامل برونشکتازی بوده باشند یا برای شناسایی عوامل بیماری زای باکتریایی خاص در طی تشدید بیماری کشت داد. هنگامیکه تشیخص برونشکتازی مسجل شد، بررسی برای تعیین علت زمینهای باید انجام شود مثل ارزیابی سطح ایمونوگلبولینها جهت بررسی نقص ایمنی متغیر ترکیبی.
تشخیص افتراقی شامل برونشیت مزمن و COPD آسم و در موارد هموپتزی و چماقی شدن انگشتان، سرطان ریه است.
درمان برونشکتازی
در صورت امکان باید علت زمینهای برونشکتازی را درمان کرد. انسداد آناتومیک مثل جسم خارجی یا تومور خوشخیم باید رفع شود. به دنبال مسجل شدن تشخیص عفونت با ایکوباکتریومهای غیر معمول توسط گستره و کشتهای متعدد باید آن را با رژیم چند دارویی مناسب درمان کرد. آسپرژیلوز برونشی-ریوی حساسیتی به طور معمول با کورتیکواستروئیدها درمان میشود، افزودن ضدقارچهای آزول نیز ممکن است مفید باشد (سطح ۳ شواهد).
آنتی بیوتیک ها
تشدیدهای باکتریایی برونشکتازی باید با آنتی بیوتیکهای گسترده طیف مؤثر علیه عوامل بیماری زای احتمالی مثل آموکسی سیلین یا در بیماران مبتلا به عفونت شناخته شده پسودوموناس یاکلونی آن، یک فلوروکینولون درمان شوند (سطح ۲). آنتی بیوتیکهای استنشاقی در سرکوب رشد باکتریها در برونشکتازی همراه بافیبروز کیستیک مفید میباشند و ممکن است در برونشکتازی غیر مرتبط با CF، در صورتی که عفونت پسودوموناس وجود داشته باشد یا تشدیدهای مکرر اتفاق بیفتد هم مفید باشد (سطح ۳). استفاده دراز مدت از ماکرولیدها التهاب و حملات تشدید را در برونشکتازی کاهش میدهد اما ممکن است سبب مقاومت باکتریایی به ماکرولیدها شود (سطح ۲).
ایمونوگلبولین ها
در افراد مبتلا به کمبود گاماگلبولینها تجویز ایمونوگلبولینها به صورت مکمل ممکن است به دفاع میزبان در برابر عفونتهای باکتریایی کمک کنند. پاکسازی راههای هوایی و تخلیه وضعیتی ترشحات به طور رایج در برونشکتازی مورد استفاده قرار میگیرند. گشادکنندههای برونش ممکن است باعث رفع علایم شوند. خلط خونی حجیم باید با محافظت از راه هوایی و شناسایی محل خونریزی درمان شود؛ ممکن است آنژیوگرافی شریان برونشیال با فرستادن آمبولی و مسدود ساختن رگ خونریزی دهنده حیات بخش باشد (سطح ۳). نقش جراحی عمدتاً برداشتن یک قطعه شدیدا آسیب دیده منفرد از ریه دچار برونشکتازی، برداشتن ضایعات انسداد دهنده که باعث برونشکتازی دیستال شدهاند، و گهگاه به عنوان درمان نجات بخش به صورت برداشتن محل خونریزی غیرقابل کنترل میباشد (سطح ۳).
فیبروز کیستیک
تعریف و اپیدمیولوژی
فیبروز کیستیک یک اختلال ژنتیک اتوزوم مغلوب است که ناشی از جهش در ژن CFTR بوده و در حدود ۳۰۰۰۰۰کودک و بزرگسال را در ایالات متحده گرفتار میکند. این بیماری بسیاری از اعضا از جمله ریهها، پانکراس، و اندامهای تولید مثل را درگیر میکند گرچه بیشتر مرگ و میر ناشی از فیبروز کیستیک در اثر درگیری ریه میباشد. این بیماری شایعترین اختلال ژنتیک مرگ آور در جمعیت سفید پوستان میباشد؛ فراوانی ناقلین ژن ۱ در ۲۹ است که یک مورد از هر ۳۳۰۰ تولد زنده را درگیر میکند.
سالیانه ۱۰۰۰ مورد جدید فیبروز کیستیک تشخیص داده میشوند. گرچه بیشتر بیماران در کودکی تشخیص داده میشوند تشخیص در برخی بیماران تا بزرگسالی به تأخیر میافتد. در حدود ۴۵٪ جمعیت مبتلا به فیبروز کیستیک در ایالات متحده بالای ۱۸ سال هستند. قبل از ۱۹۴۰، نوزادان مبتلا به فیبروز کیستیک ندرتا تا اولین سالگرد تولد خود زنده میماندند. در حال حاضر میانگین طول عمر تخمینی برای فرد مبتلا به فیبروز کیستیک در حدود ۳۷ سال است.

پاتولوژی
فیبروز کیستیک از جهش پاتوژنیک در هر دو الل یک ژن منفرد حاصل میآید که تنظیم گر هدایت کننده خلال غشایی فیبروز کیستیک (CFTR) را رمزگذاری میکند؛ این پروتئین یک کانال کلر قابل تنظیم با آدنوزین تک فسفاته حلقوی است که در سطح رأسی سلولهای اپی تلیومی وجود دارد. شایعترین جهش، AF508 میباشد که حذف شدگی سه جفت باز را در پی دارد که منجر به فقدان فنیل آلانین در جایگاه ۵۰۸ پروتئین میگردد. با این وجود تا به امروز بیش از ۱۶۰۰ جهش شناسایی شدهاند.
پروتئین غیرطبیعی CFTR منجر به نقص در نقل و انتقال کلر و افزایش باز جذب سدیم در اپیتلیوم راههای هوایی و مجاری میگردد؛ این امر باعث به وجود آمدن ترشحاتی در مجاری تنفسی، کبدی – صفراوی، گوارشی، و ولید مثلی میگردد که به طور غیرعادی غلیظ و چسبناک میباشند. ترشحات غلیظ به آسانی از راههای هوایی پاک نمیشوند و منجر به علایم تنفسی میگردند؛ این ترشحات در سایر اندامها نیز موجب انسداد و تخریب مجاری برون ریز میشوند که منجر به اختلال عملکرد اعضای برون ریز میگردد. مانند آسیب به پانکراس.
راههایی هوایی در مبتلایان به فیبروز کیستیک در ابتدا با استافیلوکوک طلایی یاهموفیلوس آنفلونزاکولونیزه میشوند و بدنبال آن و در سالهای آتی پسودومونا آیروژینوزا نیز علاوه میگردد. التهاب و عفونت پایدار موجب تخریب دیواره برونشها و برونشکتازی میگردد. انسداد راههای هوایی کوچک با توپیهای موکوسی منجر به اتساع کیستی پس از انسداد و تخریب پارانشیم میگردد و نهایتاً انسداد پیشرونده در برابر جریان هوا و هیپوکسمی عارض میگردد. مضافه، ممکن است سیر بیماری در اثر ایجاد آسپرژیلوز برونشی-ریوی حساسیتی و عفونتهای مایکوباکتریومی غیرسلی عارضه دار گردد. کولونیزه شدن و عفونت با بورخولدریا سپاسیای مقاوم به داروهای متعدد ممکن است در موارد بیماری پیشرفته رخ داده و مشکلات درمانی چالش برانگیزی پیش رو قرار دهد. بیشتر بیماران در اثر نارسایی تنفسی فوت میکنند.
تظاهرات بالینی
برنامه غربالگری نوزادان برای CF به منظور شناسایی نوزادان با احتمال ابتلا به CF در سراسر ایالات متحده انجام میگیرد. نوزادان مشکوک باید تحت ارزیابی بیشتر (تعیین ژنوتیپ) قرار گیرند.
شیرخواران مبتلا ممکن است با ایلئوس مکونیوم یا نارسایی رشد همراه با اسهال چرب تظاهر یابند. ممکن است مراقبین بچه متوجه شوری پوست وی شوند. مبتلایان به فیبروز کیستیک به طور معمول دچار سرفه مزمن همراه با تولید خلط غلیظ، خس خس، و تنگی نفس هستند. نارسایی پانکراس و دیابت شایع بوده و بیماران مرد اسپرم زنده ندارند. پولیپهای بینی شایع بوده و چماقی شدن انگشتان معمول میباشد. فیبروز کیستیک باید در تشخیص افتراقی مبتلایان به بیماری مزمن غیرقابل توجیه سینوس، برونشکتازی، ناباروری در مردان همراه با فقدان مجرای سپرم برا، پانکراتیت، یا سوء جذب مطرح گردد. آزمونهای عملکرد ریوی نشان دهنده پرهوایی و انسداد هستند؛ ممکن است پاسخ به گشادکننده برونش دیده شود. مطالعات تصویربرداری از ریه پرهوایی، ضخیم شدگی دیواره برونش، و برونشکتازی را نشان میدهند.
تشخیص و ارزیابی بالینی
فیبروز کیستیک با اندازهگیری غلظت کلر عرق (تست عرق) تشخیص داده میشود. در صورتی که تابلوی بالینی منطبق با فیبروز کیستیک باشد و غلظت کلر اندازهگیری شده در یک آزمایشگاه معتبر حداقل در دو نوبت بیش از mEq/L 60 باشد تشخیص قطعی تلقی میشود. در صورتی که تست عرق مبهم باشد میتوان با تعیین ژنوتیپ، در صورتی که جهش در هر دو الل ژن شناسایی شوند به تشخیص قطعی رسید.
درمان درمان فیبروز کیستیک برمبنای اقدامات حمایتی مانند بهداشت تهاجمی راه هوایی، حمایت تغذیهای شامل جایگزینی آنزیمهای پانکراس، آنتی بیوتیک، و گشادکنندههای برونش قرار دارد. DNAase انسانی نوترکیب استنشاقی (دُرناز آلفا) چسبندگی خلط را کاهش داده، عملکرد ریهها را بهبود بخشیده، و از تشدیدهای بیماری میکاهد. محلول نمکی (سالین) هیپرتونیک استنشاقی به آب دار کردن ترشحات کمک کرده و امکان میدهد تا به سادگی با سرفه خارج شوند، و نیز عملکرد ریوی را بهبود میبخشد گرچه احتمالاً کمتر از درناز آلفا مؤثر است (سطح ۲).
توبرامایسین استنشاقی دو مرتبه در روز یک ماه در میان در موارد فیبروز کیستیک متوسط تا شدید که دچار عفونت پسودومونایی هستند مورد استفاده دارد (سطح ۱). از ترونام استنشاقی هم در این دسته از بیماران مفید است سطح ۲). درمان ضدالتهابی با ایبوپروفن و آزیترومایسین ممکن است در بیماران خاص مفید باشد (سطح ۲ برای هر دو). با این حال مفید بودن کورتیکواستروئیدهای استنشاقی روشن نیست (سطح ۱)
درمان اختصاصی با هدف بهبود عملکرد کانال کلر معیوب CFRT تحت بررسی است. مطالعات اخیر نشان داده است که در بیمارانی که جهش خاصی از CF را دارند (G551D)، داروی ivcaftor اثرات مثبتی روی عملکرد CFRT و FEV۱ داشته است. همانند سایر بیماریهای انسدادی ریه، درمان نهایی در مبتلایان به فیبروز کیستیک که دچار بیماری مرحله انتهایی ریه هستند پیوند ریها میباشد؛ در این شرایط پیوند دوطرفه ریه ترجیح داده میشود.
آسم
تعریف و اپیدمیولوژی
آسم بر اساس تعریف GINA اختلال التهابی مزمن راههای هوایی است که در آن سلولها و عوامل سلولی زیادی نقش دارند. التهاب مزمن با واکنش دهی بیش از حد راههای هوایی همراه است که سبب حملات راجعه خس خس، تنگی نفس، تنگی قفسه سینه و سرفه (به ویژه در شب یا اوایل صبح) میشود. این حملات معمولاً با انسداد گسترده اما متغیر هوا در در داخل ریه همراه بوده و اغلب خود به خود یا با درمان بهبود مییابند (برگشت پذیرند).

بروز آسم در کودکان بیشتر است، اما همه گروههای سنی در سرتاسر دنیا ممکن است مبتلا شوند، بیماری در کشورهای توسعه یافته صنعتی شایعتر است. آسم میلیونها نفر از مردم سراسر جهان را تحت تأثیر قرار میدهد. در ایالات متحده در سال ۲۰۰۸، بر اساس بررسیها تخمین زده شد که ۲/۸% از جمعیت (تقریباً ۲۴ میلیون نفر مبتلا به آسم بودهاند که نسبت به سال ۲۰۰۱، ۳/۷% افزایش داشت. شیوع آسم طی دهههای اخیر افزایش قابل ملاحظهای داشته است. با وجود این پس از افزایشی که در اواخر قرن بیستم رخ داد، مرگ و میر ناشی از آسم از سال ۲۰۰۰ کاهش یافت، در سال ۲۰۱۰، ۳۴۰۸ مورد مرگ ناشی از آسم در ایالات متحده وجود داشت در حالیکه این تعداد در سال ۱۹۹۵، ۵۶۳۷ نفر بود. میزان مرگ و میر در سالمندان، زنان و سیاه پوستان بیشتر است.
پاتولوژی
التهاب مزمن زمینهای راههای هوایی سازوکار عمده بیماریزایی در ایجاد آسم تلقی میگردد. بیماران دچار آسم تعداد بیشتری سلول التهابی فعال درون دیواره راههای هوایی دارند و اپیتلیوم به طور بارز با ائوزینوفیلها، ماست سلها، ماکروفاژها، و لنفوسیتهای T ارتشاح یافته است که واسطههای محلول متعددی (مثل سیتوکینها، الکوترینها، برادی کینین ها) را تولید میکنند. به هر حال، با وجودی که التهاب راههای هوایی در آسم عموماً با پاسخ نوع T2 همراه با التهاب غالب آئوزینوفیلی مشخص میگردد اما برخی بیماران مبتلا به آسم شدید، التهاب نوتروفیلی راههای هوایی و تولید سیتوکینهایی را بروز میدهند که بیشتر مشخصه التهاب نوع TH۱ میباشد.
نشانه های شاخص آسم
نشانه شاخص آسم، افزایش پاسخدهی راههای هوایی است، یعنی تمایل عضلات صاف راههای هوایی برای انقباض در پاسخ به سطوحی از عوامل حساسیت زای استنشاقی که به طور معمول چنین پاسخی را در میزبان عادی بر نمیانگیزد. عوامل حساسیت زای استنشاقی با اتصال و ایجاد پیوند متقاطع بین ایمونوگلبولین های E موجود در سطح ماست سلها باعث برانگیختن تخلیه گرانولهای ماست سلهای راههای هوایی میگردند. تخلیه گرانولهای ماست سلها منجر به رهاشدن واسطههای شیمیایی میگردد که باعث اسپاسم حاد برونش و نتیجتا افزایش مقاومت راههای هوایی و خس خس، و نیز افزایش ترشح موکوس میگردد. مضافاً، به دنبال مواجهه با آنتی ژن، از هم گسیختگی یکپارچگی اپیتلیوم استوانهای مژکدار و افزایش عروق و ادم دیواره راههای هوایی رخ میدهد. در افراد مبتلا به آسم علاوه بر مواد حساسیت زا، عواملی نظیر انگیزش گیرندههای تحریکی، عفونتهای تنفسی، و سرد شدن راههای هوایی نیز میتوانند باعث برانگیخته شدن انقباض برونش گردد. به نظر میرسد سرد شدن راههای هوایی مسؤول انقباض برونش ناشی از ورزش و نیز برخی حملات آسم در فصل زمستان باشد.
آسم با بازآرایی دیواره راههای هوایی همراه است که مشخصه آن هیپرپلازی و هیپرتروفی سلولهای عضلانی صاف، ادم، ارتشاح التهابی، رگزایی، و افزایش انباشت اجزای بافت همبند همچون کلاژنهای نوع I و III میباشد. مورد آخر نه تنها منجر به ضخیم شدگی لایه مشبک زیر اپیتلیوم میشود بلکه باعث وسعت یافتن کل دیواره راه هوایی نیز میگردد. باز آرایی راههای هوایی ممکن است نسبتاً زود در سیر بیماری آغاز گردد. اینکه آیا التهاب منجر به بازآرایی میگردد یا این روند نمایانگر دو تظاهر مستقل بیماری میباشند معلوم نیست. به نظر میرسد عملکرد ریوی با سرعت بیشتری در طول زمان در بیماران مبتلا به آسم افت میکند و ممکن است بازآرایی دیواره راههای هوایی در این افت عملکرد نقشی ایفا کند. در طول زمان، ممکن است بازآرایی دیواره راههای هوایی منجر به محدودیت غیرقابل برگشت جریان هوا گردد که میتواند با کاهش اثربخشی داروهای گشادکننده برونش بر وخامت بیماری بیافزاید: بازآرایی دیواره راههای هوایی میتواند تمایز بین آسم و COPD را دشوار سازد.
دلایل آسم
علت آسم ناشناخته است اما احتمالاً یک بیماری چند ژنی است که تحت تأثیر عوامل محیطی قرار دارد. آتوپی قویا با آسم مرتبط است. آسم عموماً با یک فعالیت نوع حساسیتی در سیستم ایمنی با مشخصه پاسخدهی به آنتی ژنهای استنشاقی توسط سلولهای آباغلبه سلولهای T کمکی زیرگونه ۲ (TH۲) همراه است که در نتیجه آن IgE تولید و راههای هوایی دچار التهاب ناشی از حساسیت میگردند. قرار گرفتن در معرض حساسیت زاههای خانگی مثل جانوران ریز موجود در گردوغبار ، سوسک، حیوانات خانگی پشمالو، و قارچها نیز همانند آلایندههای هوا در بیرون منزل و سایر مواد محرک مثل دود سیگار عامل مهمی میباشند.
مفهوم جاری از بیماریزایی آسم روی اختلال جابه جایی ایمنی با غلبه TH۲ به پاسخ ایمنی با غلبه TH۱ در اوایل زندگی متمرکز است. شگفت اینکه، پایداری پاسخ ایمنی TH۲ و ایجاد پاسخهای حساسیتی نامناسب ممکن است با فقدان نسبی مواجهه سیستم ایمنی با تحریکات آنتی ژنی توسط عوامل عفونی مناسب در کودکی در جهان توسعه یافته مرتبط باشد که به اصطلاح فرضیه بهداشت نامیده میشود. برای مثال، به نظر میرسد کشاورزی احتمالاً تا حدودی به خاطر افزایش مواجهه با آنتی ژنهای میکروبی برانگیزاننده پاسخ TH۱ در برابر ابتلا به آسم و بیماریهای حساسیتی محافظت کننده باشد. افزایش تماس با سایر کودکان مثلاً در مهدکودک و استفاده کمتر از آنتی بیوتیکها نیز ممکن است خطر آسم را کاهش دهد که از این فرضیه حمایت میکند. از سوی دیگر، آسم در مناطق شهری فقیرنشین که مواجهه شدید با آنتی ژنهای حساسیت زا مثل جانوران ریز موجود در گردو غبار و سوسکها وجود دارد شایع است. زمان بندی و نقش مواجهههای محیطی خاص در داخل رحم و اوایل زندگی هنوز به خوبی روشن نشده است و در حال حاضر هیچ فرضیهای که به طور کامل بیماریزایی آسم یا افزایش اخیر در بروز آن را توجیه کند وجود ندارد. تأثیر متقابل سایر جنبههای زندگی مدرن از جمله رژیم غذایی در رابطه به استعداد ابتلا به آسم در حال روشن شدن است.

چند شکلی های ژنتیکی در آسم
چند شکلیهای متعددی از جمله گوناگونی در گیرنده – آدرنرژیک که منجر به کاهش پاسخدهی به آگونیستهای بتا میشود با آسم مرتبط بودهاند. شناسایی سایر چند شکلیهای ژنتیکی مهم در آسم، فعالانه در دست تحقیق است. گرچه آسم در کودکان پسر شایعتر از کودکان دختر میباشد اما شیوع پس از بلوغ تغییر میکند و در زنان بزرگسال شایعتر از مردان است که حاکی از تأثیرات احتمالی هورمونها در بیماریزایی آسم میباشد. آسم میتواند در اثر مواجهه شغلی در افرادی که هیچ سابقه قبلی از آسم نداشتهاند نیز ایجاد شود ( آسم شغلی). مواد خاص مثل ایزوسیانات که در اسپریهای رنگ استفاده میشوند و غبار چوب درخت سدر قرمز غربی عوامل تحریک کننده قوی برای ایجاد آسم شغلی هستند. چاقی به بروز بالای آسم ربط داده شده است که از منظر افزایش شیوع چاقی مشاهده نگران کنندهای است. سازوکارهایی که ممکن است توسط آنها چاقی ایجاد آسم را تحت تأثیر قرار دهد روشن نیستند. عوامل عفونی خاص و سایر بیماریها میتوانند باعث اسپاسم حاد برونش شوند حتی در بیمارانی که تشخیص آسم ندارند. در مورد عفونتهای ویروسی، بیماری پس زنش معده به مری، و مواجهه با گازها یا بخارات وضع به همین منوال است و این اختلالات ممکن است در ایجاد یا کنترل برخی موارد آسم نقشی ایفا کنند.
تظاهرات بالینی
علایم اصلی آسم عبارت است از خس خس، تنگی نفس دورهای، تنگی قفسه سینه و سرفه. با این حال، تظاهرات بالینی آسم ممکن است از علایم متناوب خفیف تا حملات فاجعه آمیز منجر به آسفیکسی و مرگ تفاوت بسیار داشته باشند. گرچه خس خس علامت مسجل کننده (پاتوگنومونیک) آسم نیست اما در زمینه تابلوی بالینی سازگار شایعترین تشخیص، آسم میباشد. اغلب این علایم شب هنگام یا در ساعات اولیه صبح تشدید مییابند. سایر علایم همراه عبارتاند از تولید خلط و درد یا سختی قفسه سینه، ممکن است بیماران یک یا ترکیبی از علایمی را که پیشتر ذکر شد بروز دهند مثل سرفه مزمن تنها (گونه سرفهای آسم). خس خس ممکن است چند دقیقه بعد از ورزش شروع شود (تنگی برونش ناشی از ورزش). معاینه جسمانی ممکن است طبیعی بوده (در فاصله دورههای علامت دار) یا شواهدی از خس خس را نشان دهد. ممکن است رینیت یا پولیپهای بینی وجود داشته باشند. در موارد حمله حاد، پزشک باید توجه کند که آیا بیمار به دشواری تکلم میکند، از عضلات فرعی تنفس استفاده میکند، نبض متناقض دارد، تعریق دارد، و آیا دچار تغییرات وضعیت روانی از تحریک پذیری گرفته تا خواب آلودگی میباشد یا نه. در چنین بیمارانی درمان باید فوری و تهاجمی باشد.
تشخیص و تشخیص افتراقی
تشخیص آسم مستلزم اثبات بیش فعالی و برگشت پذیری انسداد راههای هوایی در مقابل جریان هوا میباشد. شرح حال ممکن است برای این ارزیابی کافی باشد چون بیشتر بیماران از حملات مکرر اما قابل برگشت خس خس و سیار علایم شکایت دارند که به گشادکننده برونش پاسخ میدهد. اما اسپیرومتری برای ارزیابی محدودیت جریان هوای بازدمی به طور جدی توصیه میشود و برگشت پذیری نیز با تکرار اسپیرومتری پس از تجویز گشادکننده برونش ثابت میشود. بهبود FEV۱ حداقل به میزان ۱۲٪ و ۲۰۰ میلی لیتر پس از گشادکننده برونش نشان دهنده برگشتپذیری است. به دلیل دورهای بودن آسم، محدودیت جریان هوا در آن متغیر است و بیماران ممکن است زمانی که علایم را دارند نتوانند اسپیرومتری انجام دهند. اندازهگیری حداکثر جریان بازدمی در خانه نیز قابل انجام است و در اثبات متغیر بودن جریان بازدمی مفید است.
بسته به شرایط ممکن است انجام آزمون افزایش واکنش دهی راههای هوایی با چالش تحریک برونش ضرورت یابد. یک محرک با خاصیت تنگ کنندگی برونش به راههای هوایی بیمار وارد میگردد؛ از این میان متاکولین، از جمله شایعترین محرکهای مورد استفاده هستند. چون متاکولین که یک شکل صناعی استیل کولین است عوارض جانبی سیستمیک کمتری نسبت به هیستامین ادارد عموماً ترجیح داده میشود. میتوان از ورزش نیز جهت آغاز یک حمله استفاده کرد. گرچه بیشتر بیماران بدون در نظر گرفتن ابتلا به آسم ممکن است درجاتی از محدودیت جریان هوا در حین انجام آزمون تحریک برونش را نشان دهند، اما تشخیص بستگی به مقدار تحریک مورد نیاز برای برانگیختن این اثر دارد؛ افراد مبتلا به آسم در دوزهای بسیار کمتری نسبت به افرادی که مبتلا نیستند دچار محدودیت جریان هوا میگردند. در مورد متاکولین غلظتی که برای ایجاد ٪۲۰ کاهش FEV۱ از میزان پایه مورد نیاز است گزارش میشود. گرچه یک آزمون مثبت چالش تحریک برونش به تنهایی برای اسم تشخیصی نمیباشد اما نتیجه منفی آن عموماً برای رد تشخیص آسم کمک کننده است.
اندازهگیری حجمهای ریوی ممکن است در حین بیماری فعال نشان دهنده پرهوایی باشد اما DLCO به طور بارز طبیعی یا حتی بالا است. حین تشدید حاد آسم، گازهای خون شریانی در تعیین وضعیت تبادل گاز مفید میباشند. در صورتی که نگرانی از بابت عفونت ریوی وجود داشته باشد باید عکس سینه درخواست شود، اما تصویر برداری روتین از قفسه سینه ضروری نیست. ارتشاحهای گذرا یا مهاجر در عکس سینه بیمار مبتلا به آسم دشوار، باید احتمال آسپرژیلوز برونشی-ریوی حساسیتی را مطرح سازد. آزمایشات خونی در مبتلایان به آسم ممکن است نشان دهنده افزایش ائوزینوفیلهای خون و سطوح lgE باشد. آزمایشات پوستی ممکن است در شناسایی آنتی ژنهای داخل منزل و سایر آنتی ژنها که ممکن است حملات آسم را در یک بیمار بخصوص تسریع کند مفید باشد.
تشخیص افتراقی آسم شامل اختلالات تراشه، تومورهای مجرای تنفسی و جسم خارجی، COPD و برونشکتازی است. در بیمارانی که اولین بار با سرفه مزمن مراجعه میکنند، تشخیص افتراقی علل دیگر سرفه مزمن مثل GERD و ترشحات پشت حلق را هم شامل میشود. یک تشخیص افتراقی مهم در بیمارانی که به درمان معمول أسم پاسخ نمیدهند، اختلال طناب صوتی است.
درمان
درمان آسم نیازمند آموزش بیمار و همکاری وی میباشد. میتوان از دستگاههای ساده و ارزان قیمت اندازهگیری کننده حداکثر جریان بازدمی در منزل برای پایش انسداد در برابر جریان هوا استفاده کرد. باید یک یادداشت روزانه و برنامه مکتوب برای استفاده از علایم و اطلاعات مربوط به حداکثر جریان جهت مداخله زودهنگام در هنگام تشدید و تغییر درمان طولانی مدت برای کنترل بهینه علایم داشت. آگونیستهای کوتاه اثر بتا برای برطرف کردن سریع علایمی مثل خس خس مورد استفاده قرار میگیرند (سطح ۱ شواهد). با این حال سنگ بنای درمان نگهدارنده در همه بیماران بجز آنهایی که دچار بیماری خفیف متناوب هستند تجویز برنامه ریزی شده کورتیکواستروئیدهای استنشاقی است که در بهبود کنترل اسم بسیار مؤثراند (سطح ۱). در صورت لزوم میتوان آگونیستهای طولانی اثر بتا را نیز برای کنترل بهتر علایم افزود (سطح ۱). نباید از آگونیستهای طولانی اثر بتا به عنوان درمان تکدارویی جهت کنترل آسم استفاده کرد چون نشان داده شده که استفاده از این رویکرد درمانی التهاب راههای هوایی را کنترل نمیکند و با افزایش مرگ و میر همراه است (سطح ۱). اما این داروها برای کنترل بیشتر علایم به کورتیکو استروئیدهای استنشاقی اضافه میشود.
مهارکنندههای لکوترین
می توان از مهارکنندههای لکوترین در درمان نگهدارنده استفاده کرد (سطح ۱ شواهد)، گرچه عموماً به نظر میرسد کمتر از کورتیکواستروئیدهای استنشاقی مؤثر باشند (شکل ۴-۱۶). ترکیبات تئوفیلین ممکن است اثرات مفید اضافهتری در برخی بیماران نشان دهند اما پنجره درمانی باریک و اثربخشی متوسط این ترکیبات ارزش آنها را محدود میسازد. شواهد تازه نشان میدهد در بیمارانی که علیرغم استفاده از LABA و کورتیکو استروئیدهای استنشاقی، کنترل اسم مناسب نیست، استفاده از آنتی کولینرژیکهای طولانی اثر ممکن است فاصله زمانی تشدیدها را طولانیتر کرده و سبب اتساع بیشتر برونشها شود. در حین تشدیدهای حاد آسم از کورتیکواستروئیدهای خوراکی یا وریدی استفاده میشود گرچه باید از استفاده طولانی مدت از کورتیکواستروئیدهای خوراکی به علت عوارض جانبی مختلف همراه با تجویز طولانی مدت گلوکوکورتیکوئیدها در صورت امکان اجتناب کرد.
حساسیت زاها (آلرژنها)
اجتناب از حساسیت زاها (آلرژنها) جزو تمهیدات معقول در آسم میباشد گرچه اثرات مداخلات خاص مثل حفاظت توسط تشکهای دارای مانع جهت کاهش مواجهه با جانوران ریز موجود در گردوغبار اندک میباشد. درمان بیماریهای همراه مثل رینیت آلرژیک و بیماری پس زنش معده به مری که ممکن اسم را تشدید کنند از لحاظ بالینی میتواند در دست یابی به کنترل آسم کمک کننده باشد. در بیماران مبتلا به آسم آلرژیک استفاده از آنتی بادی تک دودمانی ضد IgE انسانی نوترکیب ممکن است در کاستن از تشدیدها مؤثر باشد (سطح ۲ شواهد). درمانهایی که هدفشان سایر سیتوکینهای درگیر در آسم است، تحت بررسی و تحقیق هستند. ترموپلاسمی برونش یک تکنیک جدید است که در آن انرژی بسامد رادیویی (رادیوفرکونسی) از طریق اندوسکوپی منتقل شده و سبب تخریب عضلات صاف راههای هوایی میشود. ماهها پس از این درمان، دفعات تشدید بیماری کاهش و کیفیت زندگی بیماران بهبود یافته است.
اسم حاد
اسم حاد شدید، یا حمله پایدار آسم یک حمله شدید اسپاسم برونش است که به درمانهای معمول پاسخ نمیدهد. چنین حملاتی ممکن است ناگهانی بوده (آسم فوق حاد) و به سرعت و قبل از آنکه بتوان به مراقبت پزشکی دسترسی پیدا کرد کشنده باشند. با این حال در اکثر موارد تاریخچهای از تنگی نفس پیشرونده در عرض ساعت ها تا روزها همراه با استفاده فزاینده از گشادکنندههای برونش وجود دارد. درمان حمله پایدار آسم باید تهاجمی و شامل استفاده از گشادکنندههای برونش از طریق نبولایزر و استروئیدهای وریدی به همراه پایش مداوم اشباع خون از اکسیژن توسط پالس اکسیمتری باشد؛ اغلب تجزیه و تحلیل گازهای خون شریانی برای ارزیابی از نظر هیپرکربی کمک کننده است. در بیمار مبتلا به آسم افزایش ,Paco نشانه شومی بوده و ممکن است حاکی از نیاز به حمایت تهویهای باشد. از تهویه غیر تهاجمی به طور موفقیت آمیز برای کاهش کار تنفس و اجتناب از لولهگذاری داخل نای در بیمارانی که دچار حملات تشدید آسم شدهاند استفاده شده است. با این وجود در برخی موارد در بیماران دچار حمله پایدار أسم لولهگذاری داخل نای و تهویه مکانیکی برای درمان نارسایی تنفسی ضروری است. تهویه مکانیکی در بیمار دچار حمله پایدار آسم میتواند بینهایت چالش برانگیز باشد و ممکن است نیازمند استفاده از داروهای فلج کننده برای کنترل الگوی تنفس و حتی استفاده از بیهوشی عمومی استنشاقی برای رفع اسپاسم برونش باشد.
منابع
Bulst As, McBurnie MA, Vollmer WM, et al, on behalf of the BOLD Collaborative Research Group International variation in the prevalence of COPD (the BOLD Study) a population-based prevalence study, Lancet 370741-750, 2007.
Burgel P-R, Bergeron A. de Blic I. et al: Small airways diseases, excluding asthma and COPD: an overview, Bar Respir Rev 22:131-147, 2013.
Decramer M. Janssens W, Miravitlles M: Chronic obstructive pulmonary disease, Lancet 37:1341-1351, 2012.
Global Intative for Asthma: GINA report: global strategy for asthma management and prevention (updated 2012), Available at: www.ginasthma.org. Accessed August 29, 2014.
Global Initiative for Chronic Obstructive Lung Disease: Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease (updated 2013), Available at: www.goldcopd.org. Accessed August 29, 2014.
Kim V, Criner GJ: Chronic bronchitis and chronic obstructive pulmonary disease, Am J Respir Crit Care Med 187-228-237, 2013.
King PT The pathophysiology of bronchiectasis, Int J COPD 4:411-419, 2009.
McDonough JE, Yuan R, Suzuki M, et al: Small airway obstruction and emphysema in chronic obstructive pulmonary disease, N Engl J Med 365:1567-1575, 2011, Mogayzel PJ, Naureckas ET, Robinson KA, et al: and the Pulmonary Clinical Practice Guidelines Committee: Cystic fibrosis pulmonary guidelines: chronic medications for maintenance of lung health, Am J Respir Crit Care Med 187 :680-689, 2013.
Pasteur MC, Bilton D, Hill AT) on behalf of the British Thoracic Society Bronchiectasis (Non-CF) Guideline Group British Thoracic Society guideline for non-CF bronchiectasis, Thorax 65:11-158, 2010.

*** گردآوری و تایپینگ توسط شرکت بنیان طب جراح ***







